


微米級(jí)和納米級(jí)材料的分離和分選對(duì)于精準(zhǔn)醫(yī)學(xué)、材料科學(xué)和單細(xì)胞分析等研究至關(guān)重要。 準(zhǔn)確、高效、快速分離微納尺度物質(zhì)可為癌癥早期診斷、生物樣本檢測(cè)和細(xì)胞篩選提供重要幫助。 其中,基于外場(chǎng)分離技術(shù)的微納米級(jí)物質(zhì)分離可以高效在線分離微納米級(jí)物質(zhì)。 和分選,廣泛應(yīng)用于微納米顆粒、外泌體和生物細(xì)胞的分離。 然而,目前大多數(shù)外場(chǎng)分離技術(shù)都存在設(shè)備繁瑣、樣品消耗量大等問(wèn)題。
微流控技術(shù)微流控芯片專(zhuān)家——蘇州文浩微流控科技有限公司是通過(guò)制作微通道和微流控芯片來(lái)操縱微小流體分離微納米級(jí)樣品成分的技術(shù)。 由于其快速檢測(cè)、高通量、在線分離、集成度高、成本低等優(yōu)點(diǎn),現(xiàn)已應(yīng)用于微納尺度材料分離分析。 它是微納米級(jí)材料分離的有效方法。 通過(guò)設(shè)計(jì)不同的微流控芯片、通道和外部附件,提高微納米級(jí)物質(zhì)的主動(dòng)場(chǎng)分離效率。 外場(chǎng)分離技術(shù)與微流控技術(shù)相結(jié)合,可實(shí)現(xiàn)微米級(jí)、納米級(jí)物質(zhì)的無(wú)損、高效、在線分離。 本文主要綜述了近年來(lái)微流控芯片上依靠流場(chǎng)、電場(chǎng)、磁場(chǎng)、聲場(chǎng)等外場(chǎng)分離技術(shù)提高微納米材料分離效率的研究現(xiàn)狀。 對(duì)顆粒等微米級(jí)、納米級(jí)物質(zhì)的分離進(jìn)行了分類(lèi)介紹,總結(jié)了各自的優(yōu)缺點(diǎn)及發(fā)展應(yīng)用。 最后對(duì)外場(chǎng)分離技術(shù)和微流控技術(shù)在癌細(xì)胞早期篩查和微尺度物質(zhì)精準(zhǔn)分離中的應(yīng)用進(jìn)行了展望。 討論了該領(lǐng)域未來(lái)的發(fā)展前景,并提出了聯(lián)合技術(shù)的優(yōu)勢(shì)和未來(lái)應(yīng)用。
微米級(jí)和納米級(jí)物質(zhì)的分離和分選在生命科學(xué)、材料科學(xué)和環(huán)境科學(xué)領(lǐng)域至關(guān)重要。 微納尺度物質(zhì)的分離將對(duì)靶點(diǎn)篩選、個(gè)體化差異化、新藥研發(fā)、個(gè)體化精準(zhǔn)治療產(chǎn)生巨大影響。 意義。 目前力和機(jī)械,對(duì)微米級(jí)和納米級(jí)物質(zhì)的分離和分選主要是根據(jù)其表面物理化學(xué)性質(zhì)的不同,如尺寸、形狀、電荷、質(zhì)量等。現(xiàn)有的分離微米級(jí)和納米級(jí)材料的方法可分為兩個(gè)主流。 一是被動(dòng)分離技術(shù),在通道和流體的共同作用下,根據(jù)目標(biāo)尺寸差異的不同路徑實(shí)現(xiàn)分離,如確定性橫向位移、慣性聚焦、超濾、離心等。雖然被動(dòng)分離技術(shù)已經(jīng)取得了一些進(jìn)展其普遍存在分離度低、通道易堵塞、難以實(shí)現(xiàn)在線分離檢測(cè)等問(wèn)題。 第二種分離方法是主動(dòng)分離技術(shù),根據(jù)混合目標(biāo)中不同目標(biāo)的不同物理化學(xué)性質(zhì),通過(guò)添加不同的外力場(chǎng)來(lái)改變目標(biāo)在分離系統(tǒng)內(nèi)的運(yùn)動(dòng)行為來(lái)實(shí)現(xiàn)分離。 外力場(chǎng)的類(lèi)型包括電場(chǎng)、磁場(chǎng)、流場(chǎng)和聲場(chǎng)。 這些主動(dòng)分離技術(shù)可以實(shí)現(xiàn)微納米尺度材料的在線分離和分選,應(yīng)用于微粒、外泌體、病毒、單細(xì)胞的分離。 展現(xiàn)出重要的作用。 然而,如何使這些分離技術(shù)小型化、集成化、易于操作仍然是當(dāng)今需要解決的問(wèn)題。
微流控技術(shù)又稱(chēng)芯片實(shí)驗(yàn)室,起源于Manz等人提出的“微全分析系統(tǒng)”。 1990年,它是指通過(guò)制作微通道或微流控芯片來(lái)操縱微小流體和分析微型材料樣品。 分離分離技術(shù)是主要針對(duì)微納尺度物質(zhì)分離的有效方法。 微流控技術(shù)實(shí)現(xiàn)了微米級(jí)、納米級(jí)物質(zhì)的精確、高通量、在線分離。 它可以用最少的試劑、時(shí)間和成本完成分離任務(wù),具有小型化、集成化、低成本、高通量的特點(diǎn)。 隨著微流控技術(shù)的發(fā)展,利用微納米尺度物質(zhì)的不同性質(zhì),制作特殊結(jié)構(gòu)的微流控芯片器件,以提高微納米尺度物質(zhì)的分離效率,并且更有針對(duì)性。 微流控芯片的生物功能兼容性提高了其在生物細(xì)胞操作和分析中的應(yīng)用。 同時(shí),在微流控技術(shù)方面,可以合理化復(fù)雜的分析方案,顯著減少樣品量和試劑成本,在處理微量樣品時(shí)具有降低成本、減少危害、降低風(fēng)險(xiǎn)的優(yōu)勢(shì)。 提高分辨率等優(yōu)點(diǎn)。 隨著微流控技術(shù)在微納米尺度物質(zhì)分離方面的不斷成長(zhǎng)和進(jìn)步,細(xì)胞、顆粒等微納米尺度物質(zhì)的分離在醫(yī)學(xué)領(lǐng)域和生物化學(xué)領(lǐng)域發(fā)揮著至關(guān)重要的作用。 利用這些優(yōu)點(diǎn),可以將基于外場(chǎng)的分離技術(shù)與微流控技術(shù)相結(jié)合,制備出所需的微流控芯片,并對(duì)不同特性的樣品施加電場(chǎng)、磁場(chǎng)、聲場(chǎng)等外力場(chǎng)來(lái)混合樣品。 組件被精確分離。
本文主要概述了微流控芯片上依靠流場(chǎng)、電場(chǎng)、磁場(chǎng)、聲場(chǎng)主動(dòng)分離技術(shù)提高分離效率的研究現(xiàn)狀,探討了生物細(xì)胞富集、混合等有效精準(zhǔn)分離的發(fā)展與應(yīng)用。顆粒物。 。
1 流場(chǎng)流動(dòng)分離技術(shù)
流場(chǎng)流動(dòng)分離技術(shù)是各種場(chǎng)流分離技術(shù)中最常用的技術(shù)。 其中,非對(duì)稱(chēng)流場(chǎng)流動(dòng)分離技術(shù)是1987年提出的流場(chǎng)分餾技術(shù),目前得到廣泛應(yīng)用。 該技術(shù)將非特異性相互作用減少到最低限度,并具有高分辨率的優(yōu)點(diǎn)。 在FIFFF通道中,外力場(chǎng)是垂直于流道方向的橫向流動(dòng)。 在橫流的驅(qū)動(dòng)下,樣品與其自身的擴(kuò)散力相互作用,二者之間達(dá)到平衡,各成分在通道內(nèi)壁上產(chǎn)生分布差異。 其中,小尺寸樣品在堆積壁上形成的分布層高于大尺寸顆粒。 此時(shí),流場(chǎng)在通道內(nèi)流動(dòng)時(shí),分布層較小。 小尺寸的顆粒比較大尺寸的顆粒更早洗脫,從而實(shí)現(xiàn)分離。 FIFFF 沒(méi)有固定相,對(duì)樣品施加的剪切力和機(jī)械應(yīng)力較小,使其成為一種溫和的分離技術(shù)。 它已被廣泛用于分離和表征不同大小和形狀的顆粒、細(xì)胞、蛋白質(zhì)或 DNA。 物質(zhì)。
竇等人。 采用非對(duì)稱(chēng)流場(chǎng)流分離技術(shù),在線耦合紫外、多角度光散射和熒光檢測(cè)器,對(duì)蛋黃血漿進(jìn)行分離和表征。 以蛋黃血漿作為AF4的載液,評(píng)價(jià)了AF4高效快速分離和表征蛋黃血漿中可溶性蛋白、低密度脂蛋白及其聚集體的實(shí)用性。 同時(shí)研究了低密度脂蛋白在卵黃血漿中的聚集行為。 使用程控錯(cuò)流AF4具有提高檢測(cè)能力、減少樣品消耗、縮短分析時(shí)間的優(yōu)點(diǎn)。 結(jié)果證明AF4適合于蛋黃血漿等粒徑分布范圍較大的目標(biāo)物的分離和表征。 該團(tuán)隊(duì)還利用AF4結(jié)合多角度光散射和差示折射探測(cè)器對(duì)淀粉的分離和表征進(jìn)行了深入研究,為今后更好地研究淀粉的結(jié)構(gòu)功能關(guān)系提供了重要信息。
阿什比等人。 利用流場(chǎng)流動(dòng)分離技術(shù)結(jié)合離心分離技術(shù),建立了基于相對(duì)解離速率的電暈蛋白鑒定方法,篩選納米粒子與蛋白質(zhì)之間的相互作用。 該方法在人血清中孵育超順磁性氧化鐵納米顆粒和免疫球蛋白G (IgG),然后使用F4和離心分離對(duì)SPION具有更好親和力的蛋白質(zhì)。 F4以更快的速度洗掉與SPION具有更好親和力的蛋白質(zhì)。 蛋白質(zhì)與納米顆粒相互作用解決了納米顆粒進(jìn)入生物基質(zhì)時(shí),基質(zhì)表面形成的蛋白電暈對(duì)納米顆粒在生物系統(tǒng)中后續(xù)行為的影響,有助于研究蛋白電暈的時(shí)間分布和它在生物基質(zhì)中的運(yùn)動(dòng)。 與顆粒特性相關(guān)的蛋白質(zhì)電暈動(dòng)態(tài)特征的進(jìn)化和高通量分析。
等人。 將納米粒子跟蹤技術(shù)與AF4耦合,得到AF4-NTA技術(shù),彌補(bǔ)了NTA在線檢測(cè)器檢測(cè)范圍窄、流量小、壓力閾值低等問(wèn)題。 AF4-NTA作為一種對(duì)混合物中不同顆粒數(shù)的納米材料進(jìn)行高效、準(zhǔn)確的顆粒計(jì)數(shù)技術(shù),采用合理的分流設(shè)計(jì),對(duì)粒徑為50、100、200 nm的聚苯乙烯混合物進(jìn)行分離分析,同時(shí)進(jìn)行在線精確顆粒計(jì)數(shù)不同納米尺寸目標(biāo)的混合物。
目前,AF4正在不斷進(jìn)步和發(fā)展,在化學(xué)分離領(lǐng)域或生命科學(xué)等其他重要領(lǐng)域展現(xiàn)出巨大的潛力。 利用分離溫和、裝置結(jié)構(gòu)簡(jiǎn)單的特點(diǎn),可以與不同的檢測(cè)器耦合。 為生物治療和納米顆粒分離表征提供技術(shù)支持。 未來(lái),AF4溫和的分離特性優(yōu)勢(shì)將與微流通道小型化、節(jié)省試劑、節(jié)省樣品成本的優(yōu)勢(shì)相結(jié)合,成為一種高度靈活、高分辨率的分離技術(shù),具有巨大的發(fā)展前景。
2 基于外電場(chǎng)的分離技術(shù)
近年來(lái),越來(lái)越多的科學(xué)家利用電場(chǎng)來(lái)分離和分析微米級(jí)和納米級(jí)材料。 主要分離原理是根據(jù)目標(biāo)物體的大小、大小、顆粒物等不同特性,通過(guò)調(diào)節(jié)電參數(shù)改變分離系統(tǒng)中的運(yùn)動(dòng)行為來(lái)控制和分離生物細(xì)胞、顆粒物等微納米級(jí)物質(zhì)。收費(fèi)。 。 常見(jiàn)的施加電場(chǎng)的分離方法分為四種(見(jiàn)圖1),即毛細(xì)管電泳、介電泳、電場(chǎng)流分離和電滲驅(qū)動(dòng)。

圖1 目前廣泛應(yīng)用的4種電場(chǎng)分離技術(shù)
2.1 毛細(xì)管電泳
根據(jù)介質(zhì)中帶電粒子在一定電場(chǎng)作用下定向遷移的性質(zhì),采用毛細(xì)管電泳技術(shù),在兩端施加高壓電場(chǎng),對(duì)微納尺度物質(zhì)進(jìn)行分離分析,以滿足當(dāng)今的要求。高效、快速的分離需求。 毛細(xì)管內(nèi)壁與緩沖溶液的界面處形成雙電層,并在高壓電場(chǎng)驅(qū)動(dòng)下形成定向電滲流。 如圖1a所示,帶電粒子根據(jù)其自身的電泳力和電滲流力之間的差異進(jìn)行分離。 毛細(xì)管電泳具有分析快速靈敏、樣品消耗少、分離效率高等優(yōu)點(diǎn)。 廣泛應(yīng)用于藥物分析、環(huán)境監(jiān)測(cè)、食品檢測(cè)等領(lǐng)域。 毛細(xì)管電泳技術(shù)與微流控技術(shù)的結(jié)合,即微流控芯片電泳,是近年來(lái)得到廣泛應(yīng)用的一種新型分離技術(shù)。 它具有成本低、分辨率高、速度快等優(yōu)點(diǎn),廣泛應(yīng)用于微米級(jí)、納米級(jí)物質(zhì)的檢測(cè)。 在分離分析中。 張等人。 利用微流控芯片電泳技術(shù)對(duì)大腸桿菌、金黃色葡萄球菌、鼠傷寒沙門(mén)氏菌三類(lèi)細(xì)菌進(jìn)行定量檢測(cè),有助于人工污染生肉中致病菌的分析。 結(jié)果表明,MCE技術(shù)具有靈敏度高、速度快、試劑消耗低、操作快速等優(yōu)點(diǎn)。 是一種有效、可靠的食品安全評(píng)價(jià)方法。
全杰恩等人。 開(kāi)發(fā)了一種基于壓力驅(qū)動(dòng)流誘導(dǎo)電泳的連續(xù)分離方法。 如圖2a所示,在微流控裝置中,混合的微納米級(jí)物質(zhì)在來(lái)自流體的驅(qū)動(dòng)力、電滲流帶來(lái)的阻力以及以電泳力為主的三種合力的作用下,按照各自的作用有效地分離。在電場(chǎng)的影響下具有電泳遷移率,分離效率可達(dá)97%。
為了驗(yàn)證常用的蒽環(huán)類(lèi)抗腫瘤藥物阿霉素是否與谷胱甘肽結(jié)合,蔡啟丹等人利用了微流控芯片電泳技術(shù)的小型化、集成化等優(yōu)勢(shì)。 如圖2b所示,采用簡(jiǎn)化芯片毛細(xì)管電泳法考察阿霉素與還原型谷胱甘肽和氧化型谷胱甘肽的親和力,最終得出谷胱甘肽本身對(duì)阿霉素沒(méi)有親和力。 該結(jié)論為抗腫瘤藥物的研發(fā)提供了理論支持。 綜上所述,毛細(xì)管電泳技術(shù)與微流控技術(shù)的結(jié)合在醫(yī)療、食品、生物等各個(gè)領(lǐng)域都具有巨大的發(fā)展前景。
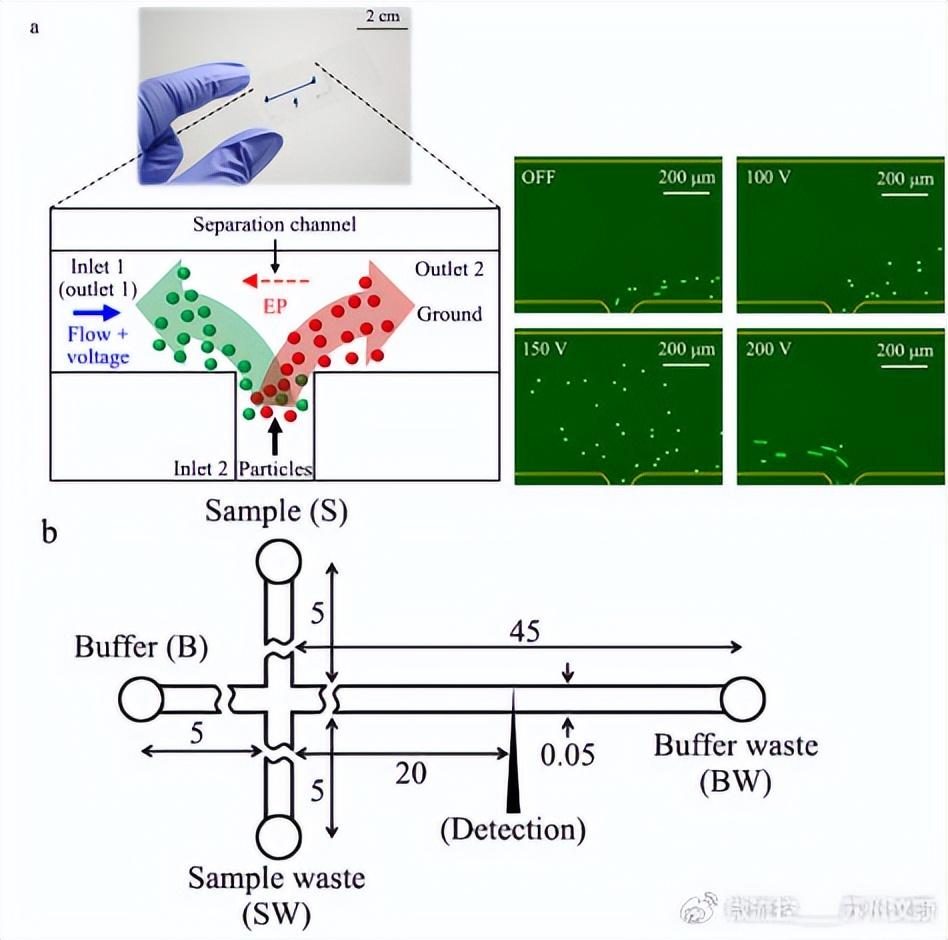
圖2 基于微流控芯片電泳的分離系統(tǒng)
毛細(xì)管電泳技術(shù)與微流控技術(shù)的結(jié)合,具有毛細(xì)管電泳技術(shù)免標(biāo)記、對(duì)細(xì)胞無(wú)損傷的優(yōu)點(diǎn)。 微流控技術(shù)的結(jié)合實(shí)現(xiàn)了高效、小型化、精密分離,解決了傳統(tǒng)毛細(xì)管電泳技術(shù)設(shè)備繁瑣的問(wèn)題。 問(wèn)題,具有廣闊的應(yīng)用前景。
2.2 介電泳
介電電泳最早由 Pohl 在 20 世紀(jì) 50 年代提出。 這意味著可極化粒子在非均勻電場(chǎng)中會(huì)被極化,產(chǎn)生偶極矩。 偶極矩和非均勻電場(chǎng)之間產(chǎn)生介電泳力。 。 該系統(tǒng)中的粒子將受到正介電泳力(指向場(chǎng)的最大力)或負(fù)介電泳力(遠(yuǎn)離場(chǎng)的最大力),如圖 1b 所示。 介電泳操作顆粒具有集成化、操作簡(jiǎn)便、成本低等優(yōu)點(diǎn),已廣泛應(yīng)用于微粒和細(xì)胞的分離。 然而,如果在強(qiáng)電場(chǎng)條件下用介電泳分離生物樣品,生物樣品會(huì)因電場(chǎng)中焦耳熱的影響而被直接殺死或不可逆地破壞。 因此,利用微流控器件低發(fā)熱、高通量、低成本等優(yōu)勢(shì),將介電泳技術(shù)與微流控技術(shù)相結(jié)合,實(shí)現(xiàn)生物樣品的無(wú)損高效分離。
為了解決多組分樣品同時(shí)富集的問(wèn)題,Zhao等人。 開(kāi)發(fā)了一種新型微流控裝置,可在直流介電泳提供的非均勻電場(chǎng)條件下調(diào)節(jié)外部電場(chǎng)的電參數(shù)和流動(dòng)相懸浮液的電導(dǎo)率。 ,實(shí)現(xiàn)尺寸相似但介電性能不同的微納混合顆粒的分離。
趙等人。 還生產(chǎn)了新型AC介電泳微流控芯片。 該芯片同時(shí)將兩個(gè)電極嵌入相對(duì)側(cè)壁上的一組不對(duì)稱(chēng)孔中,以產(chǎn)生不均勻的電場(chǎng)。 如圖3a所示,當(dāng)生物細(xì)胞和其他樣品通過(guò)微流控裝置時(shí),利用液體聚焦使樣品在同一水平線上移動(dòng)。 當(dāng)聚焦的樣品進(jìn)入DEP電場(chǎng)范圍時(shí),樣品在兩個(gè)方向上受到pDEP和nDEP的影響。 移動(dòng)到側(cè)孔內(nèi)。 本實(shí)驗(yàn)研究了活酵母細(xì)胞和死酵母細(xì)胞在不同離子濃度、電導(dǎo)率和交流電場(chǎng)頻率下的 DEP 行為。 與直流介電電泳不同,該裝置利用交流頻率和電壓等參數(shù),成功分離大小相似但介電常數(shù)不同的活酵母細(xì)胞和死酵母細(xì)胞。 該微流控裝置制造簡(jiǎn)單力和機(jī)械,旨在避免焦耳熱效應(yīng),并且可以誘導(dǎo)非均勻電場(chǎng)產(chǎn)生強(qiáng)梯度,可用于分離相似尺寸的納米顆粒。
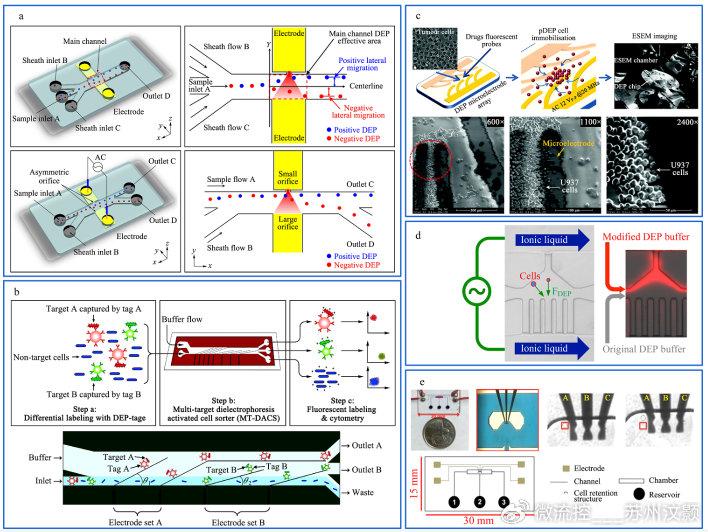
圖3 基于介電泳技術(shù)的微流控分離系統(tǒng)
金等人。 使用獨(dú)特的合成介電泳標(biāo)記來(lái)識(shí)別多種細(xì)胞類(lèi)型,在微流控裝置的內(nèi)部通道結(jié)構(gòu)上放置兩個(gè)不同角度的傾斜電極,并利用傾斜電極提供非均勻電場(chǎng),如圖3b所示。 在非均勻電場(chǎng)下,混合樣品中不同尺寸的顆粒在裝置中產(chǎn)生不同的運(yùn)動(dòng)行為,實(shí)現(xiàn)高分辨率和高通量的分離效果。
設(shè)計(jì)了一種非粘附性脂質(zhì)捕獲DEP系統(tǒng),如圖3c所示,利用光刻技術(shù)在玻璃基板上制備DEP微電極陣列,以避免生物細(xì)胞的污染。 基于芯片的陣列用于捕獲人類(lèi)白血病細(xì)胞的環(huán)境掃描電子顯微鏡分析。 這項(xiàng)工作驗(yàn)證了 DEP 細(xì)胞保留和捕獲技術(shù)。 利用DEP芯片捕獲人白血病細(xì)胞,并在ESEM上對(duì)單個(gè)非貼壁細(xì)胞進(jìn)行高分辨率分析,實(shí)現(xiàn)造血腫瘤和干細(xì)胞的流體動(dòng)力學(xué)捕獲和長(zhǎng)期動(dòng)態(tài)分析。
孫等人。 開(kāi)發(fā)了一種具有自組裝液體電極的新型DEP微流控裝置,如圖3d所示。 由室溫離子液體形成的液體電極與DEP緩沖溶液耦合,然后利用外部電場(chǎng)施加的電壓來(lái)增加微流控芯片內(nèi)的電導(dǎo)率并產(chǎn)生電場(chǎng)梯度,以有效分離細(xì)胞和顆粒。芯片。 組裝的液體電極DEP微流控裝置成功分離了聚苯乙烯珠和PC-3細(xì)胞、存活和凋亡的PC-3細(xì)胞、人類(lèi)脂肪干細(xì)胞和MDA-MB-231癌細(xì)胞。 該裝置具有成本低、分離效率高等優(yōu)點(diǎn),在細(xì)胞分離實(shí)驗(yàn)中具有巨大潛力。
使用介電泳來(lái)操縱懸浮在液體介質(zhì)中的可極化粒子,并使用介電泳芯片制作了一個(gè)裝置,如圖3e所示。 微流控芯片通道內(nèi)部充滿藍(lán)色染料,細(xì)胞樣本從左側(cè)入口注入。 中間的儲(chǔ)液器用于藥物輸送,在電極產(chǎn)生的介電泳力的作用下捕獲骨髓白細(xì)胞。 采用介電泳芯片裝置對(duì)單細(xì)胞進(jìn)行分析,檢測(cè)單細(xì)胞在多藥耐藥的藥物流出功能中的異質(zhì)性,捕獲具有MDR活性的白血病細(xì)胞和不具有MDR活性的白血病細(xì)胞,將其與良性白細(xì)胞區(qū)分開(kāi)來(lái)。 。 這為未來(lái)的醫(yī)學(xué)試驗(yàn)研究提供了一種新技術(shù),可以在單細(xì)胞水平上確定 MDR 抑制的異質(zhì)性。
綜上所述,介電泳技術(shù)對(duì)于尺寸相似、節(jié)點(diǎn)特性差異較小的微納米級(jí)物質(zhì)的分離不具備高分辨率,且傳統(tǒng)介電泳裝置在高電壓條件下容易對(duì)生物細(xì)胞造成損傷。 同時(shí),有效電場(chǎng)較小,因此介電泳技術(shù)可以與微流控技術(shù)相結(jié)合。 微流控技術(shù)裝置的小型化設(shè)計(jì)可在低電壓條件下產(chǎn)生更高的有效電場(chǎng)。 精確分離具有獨(dú)特特性的混合樣品。