缺血再灌注損傷(,IRI)指經過一定時間缺血的組織臟器再恢復血液灌注后其代謝、功能及結構的損傷反倒加重,甚至出現不可逆性損傷的現象[1]。IRI發生較為常見,在心肌梗塞、腦卒中、肺和腎等移植放療后均可發生,因而研究IRI的病理生理及其發生機制具有重大臨床意義。目前研究覺得IRI發生的兩個主要機制是細胞內鈣超員和活性氧簇(,ROS)形成過多,尤其是細胞內鈣超員[2],故怎么降低細胞內鈣超員對減少IRI具有重大作用。近些年來細胞電生理研究結果表明,除了線粒體ATP敏感性鉀通道開放可降低細胞內鈣超員,減少IRI[3],但是大濁度鈣激活鉀通道(BKCa通道)開放同樣可減少IRI[4],甚至其減少IRI的作用比ATP敏感性鉀通道更強[5],故本文主要綜述BKCa通道在IRI中的作用及其機制。
一、BKCa通道的基本特點
1.BKCa通道的通常特點和生理功能:
BKCa通道廣泛分布于血管平滑肌細胞上,我們前期研究結果表明,BKCa通道電壓約占冠狀動脈血管平滑肌細胞總鉀離子流的65%[6]。BKCa通道為200~300pS,激活具有電流依賴性和鈣離子(Ca2+)含量依賴性[7]。BKCa通道由4個α和4個β亞單位組成,每位α亞單位結合1個β亞單位,產生BKCa通道四聚體結構。α亞單位由基因編碼,包括與細胞外羥基端相連的7個跨膜片斷(S0~S6),以及坐落細胞內與酸酐端相連的4個疏水性片斷(S7~S10)。β亞單位是兩次跨膜蛋白,胞外有近120個多肽殘基組成的肽鏈將兩個跨膜段聯接,其胺基端和甲基端均在細胞內。β亞單位有4種亞型,在血管平滑肌細胞中主要是β1亞單位,由基因編碼。BKCa通道參與血管平滑肌細胞靜息膜電位和血管張力的調節[8]。使用BKCa通道興奮劑可使細胞膜超極化,血管舒張;相反,使用BKCa通道阻滯劑可使細胞膜去極化,血管收縮[9]。
2.BKCa通道興奮劑和阻滯劑:
BKCa通道興奮劑主要分為三大類:(1)內源性物理物質,如玉米四油酸、17β-孕酮和n-3多不飽和脂肪酸等,可以降低BKCa通道活性,調節血管張力[10];(2)天然BKCa通道興奮劑,如DHS-I(-I),可顯著降低血管平滑肌細胞BKCa通道開放機率[11];(3)人工合成的BKCa通道興奮劑,如NS004、、等,雖然這種化合物目前仍未應用于臨床,但卻是研究BKCa通道功能重要的工具。
BKCa通道阻滯劑包括美洲蝎毒索、蕈抗生素、北非蝎毒素等,其中肯尼亞蝎毒索和蕈抗生素是最常用的BKCa通道阻滯劑[12]。在研究BKCa通道的結構特點以及在不同的生理狀態下BKCa通道激活機制時,BKCa通道阻滯劑發揮重要作用。
二、IRI的發生機制
IRI的發生機制目前尚不完全清楚,目前較多公認的機制有鈣超員、ROS大量積聚和堿性代謝產物增多等誘因。
1.鈣超員:
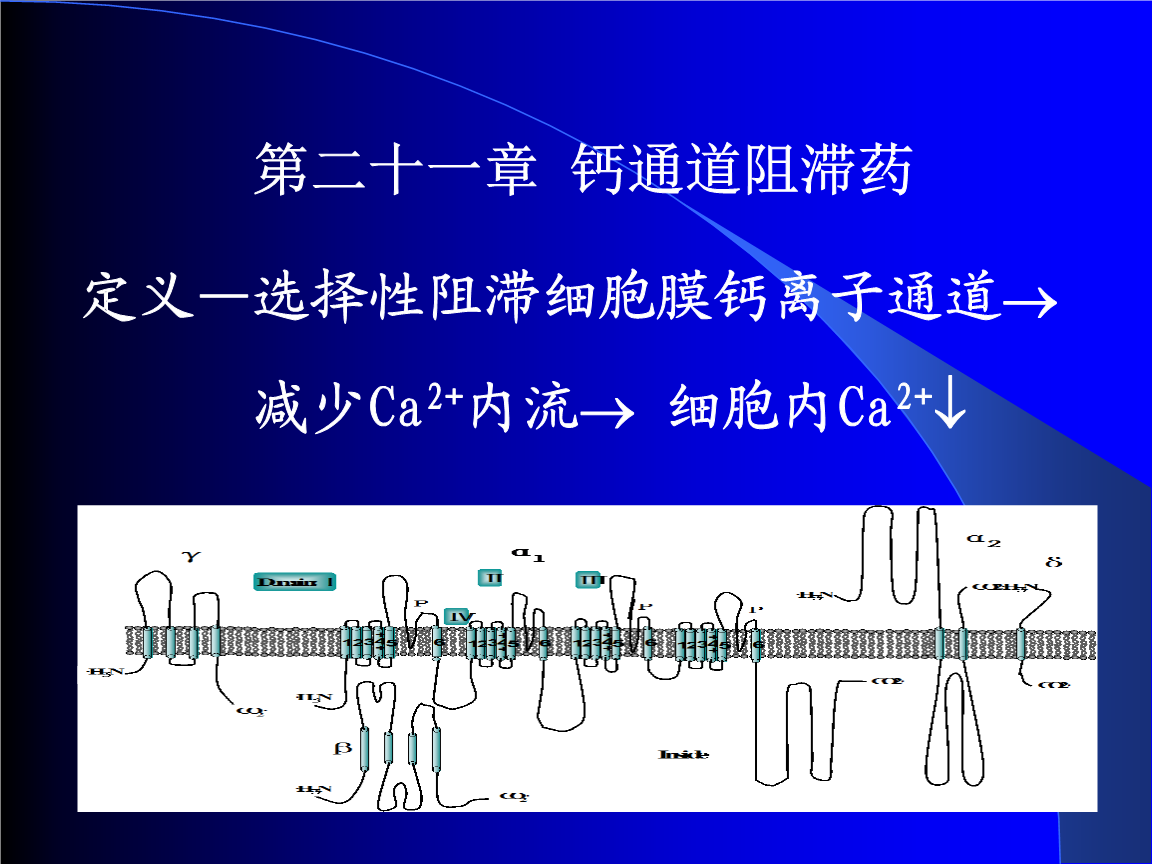
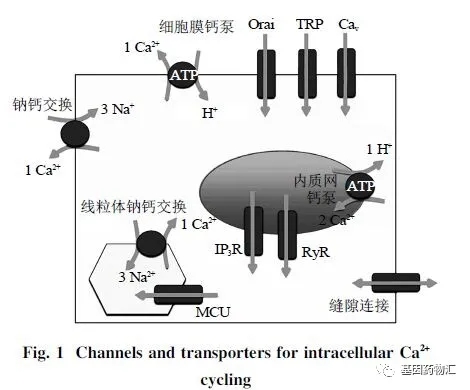
生理狀態下胞漿內Ca2+含量與細胞外液中Ca2+含量相差10000倍左右。細胞的肌漿網、內質網和線粒體都是細胞內Ca2+的儲存庫,這些Ca2+穩態維持依賴于一系列Ca2+的轉運機制。組織臟器缺血時鈉離子鉀離子通道阻滯劑,細胞內ATP形成降低,鈉泵活性增加,導致細胞內Na+積聚,細胞腫脹;再灌注時,細胞內高含量Na+迅速激活Na+/Ca2+交換體,使Na+外流,同時大量Ca2+步入細胞內,導致細胞結構損傷和功能代謝障礙,這是缺血再灌注鈣超員產生的主要途徑[13]。鈣超員可以造成細胞膜、線粒體和肌漿網膜損傷,降低膜的私密性,使內皮細胞腫脹;鈣超員還可以提高鈣依賴性蛋白酶活性,加速黃固醇酯化酶轉化為黃固醇氧化酶,促使更多自由基生成,損傷組織。
2.ROS大量積聚:
ROS分為羥自由基、過氧化氫和超氧離子自由基等。在正常生理條件下,機體自身不斷形成ROS,又不斷消除ROS,使其維持在一個動態平衡之中。但缺血再灌注時,機體形成ROS增多,而消除相對降低,進而造成大量ROS在細胞內堆積。ROS具有強悍的氧化活性,對幾乎所有的生物分子都有損傷,尤其是對脂類最為敏感。ROS與細胞膜、線粒體膜及溶酶體膜上的不飽和脂肪酸發生脂類二溴化作用,形成二溴化脂類可以損傷生物膜。ROS使脂類發生二溴化反應,改變膜滲透性,又促使更多Ca2+內流;ROS還破壞線粒體結構,干擾氧化乙酸化過程,加速ATP等高能乙酸化合物潰散,使ATP依賴的離子泵活性增長,其結果是進一步推動細胞內Ca2+降低,引起鈣超員。而鈣超員又激化氧自由基的生成,兩者互相影響,協同作用,最終造成IRI進一步加重。
3.堿性代謝產物增多:
組織臟器缺血,能量代謝障礙,細胞無氧代謝,使細胞內H+生成增多,激活Na+/H+交換蛋白,Na+內流增多,從而間接激活Na+/Ca2+交換蛋白,造成細胞內Ca2+含量下降鈉離子鉀離子通道阻滯劑,加重細胞內鈣超員[14]。再灌注前或再灌注即刻應用鈣拮抗劑、Na+/H+交換蛋白或Na+/Ca2+交換蛋白抑制劑可抑制細胞內鈣超員,減少IRI[1]。
三、BKCa通道對IRI的保護作用
1.缺血再灌注時BKCa通道電壓的變化:
Han等[15]采用膜片鉗實驗技術研究缺血再灌注時BKCa通道電壓的變化。研究分為實驗組和對照組,其中實驗組為缺血1h后豬冠狀動脈平滑肌細胞,對照組為正常豬冠狀動脈平滑肌細胞。結果發覺實驗組BKCa通道電壓顯著升高;同時給與BKCa通道興奮劑,發覺實驗組BKCa通道電壓的降低幅度高于正常對照組(P[16]研究同樣發覺缺氧狀態下,人肺動脈平滑肌細胞BKCa通道活性增長,且BKCa通道亞單位抒發減低。那些研究表明缺血再灌注時BKCa通道功能損壞可能是IRI發生的重要機制之一。
2.BKCa通道興奮劑激活BKCa通道可減少IRI:
等[17]首次發覺腦膠質瘤細胞線粒體內膜上有BKCa通道,且和冠狀動脈平滑肌細胞BKCa通道的基因抒發相同,均為基因[18]。采用BKCa通道興奮劑處理再灌注腎臟后,心肌梗塞面積顯著降低,表明心肌細胞線粒體BKCa通道開放時,對IRI心肌具有保護作用[19,20]。為明晰是通過激活BKCa通道,而不是通過興奮線粒體ATP敏感性鉀通道所起作用,Redel等[21]在用處理再灌注腎臟同時,加入線粒體ATP敏感性鉀通道抑制劑,發覺的保護作用依然存在,而加入BKCa通道阻滯劑,保護作用消失,提示是通過激活心肌細胞線粒體內膜BKCa通道,而不是通過激活線粒體ATP敏感性鉀通道起作用。
但是,上述研究似乎排除不是通過激活線粒體ATP敏感性鉀通道起作用,但尚不能排除激活其他離子通道發揮作用。等[22]采用對BKCa通道激活特異性更高且中單粒體ATP敏感性鉀通道無作用的興奮劑在心肌缺血前進行預處理,結果同樣發覺BKCa通道興奮劑對心肌IRI具有保護作用,且在一定含量范圍內,對IRI的保護作用與含量呈正相關,1和3μmol/L的降低心肌梗塞后面積分別為(11.4±2.0)%和(20.6±4.5)%(PCa通道激活對IRI具有保護作用,表明BKCa通道可能是IRI潛在醫治靶向。與既往研究不同的是,該研究結果表明BKCa通道興奮劑對缺血后心肌同樣具有保護作用,但保護作用相對較弱。
近些年來,等[18]和等[23]采用基因敲除技術進一步闡述BKCa通道在IRI中的保護作用。結果表明,采用BKCa通道興奮劑預處理正常腎臟,心肌梗塞面積顯著降低,但同樣采用BKCa通道興奮劑預處理敲除BKCa通道基因的腎臟,心肌梗塞面積降低,因而充分否認激活BKCa通道可減少IRI,即IRI時可通過激活BKCa通道而起保護作用。以上基因敲除技術的使用,是現今實驗技術的重大進展,明晰了BKCa通道在IRI中的保護作用。
3.缺血預處理激活BKCa通道減少IRI:
缺血預處理指一次或多次非損傷性、短暫、重復的心肌缺血和再灌注,能增強心肌對隨即發生的長時間缺血損傷的耐受能力。早在1986年,美國就有研究報導覺得缺血預處理對于不同組織臟器的IRI具有保護作用,但其機制尚不清楚。李向東等[24]也發覺缺血預處理可減少豬急性心肌梗塞再灌注后心肌無復流和再灌注損傷。等[25]在缺血預處理過程中加入BKCa通道阻滯劑發覺缺血預處理作用增加,心肌梗塞面積降低;但如只在再灌注過程中加入抑制劑,缺血預處理作用依然存在。這提示缺血預處理的保護作用可能是在缺血初期提升了BKCa通道活性,而不是在后期的再灌注過程中。等[18]也借助基因敲除技術進行研究,發覺在缺血預處理狀態下,BKCa通道基因敲除大鼠腎臟與正常對照組腎臟梗塞面積分別為(58±5)%和(28±3)%(PCa通道實現的。為此,BKCa通道可能是缺血預處理減少IRI的離子機制之一。
四、BKCa通道對IRI的保護作用機制
BKCa通道興奮劑激活BKCa通道對IRI的保護作用機制主要是通過降低鈣超員和ROS大量積聚。Kang等[5]借助鈉泵阻滯劑哇巴因完善小鼠腎臟鈣超員模型,再用BKCa通道興奮劑灌注小鼠腎臟,發覺線粒體Ca2+含量增加。這是因為BKCa通道激活后,K+內流,線粒體膜去極化,增加了Ca2+內流的電物理梯度,抑制或延后Ca2+內流,減少鈣超員現象。當加入BKCa通道阻滯劑后,Ca2+含量上升,說明BKCa通道可以通過增加鈣超員來減少IRI。BKCa通道增加鈣超員的過程受蛋白激酶A調節。與蛋白激酶A興奮劑聯合應用時,其作用提高;而單獨使用蛋白激酶A興奮劑,對BKCa通道無激活作用[21]。等[26]用灌注腎臟發覺H2O2釋放率由(85±25)%降到(12±1)%,因而得出BKCa通道興奮劑可降低ROS形成的推論。等[27]同樣也否認BKCa通道興奮劑能降低ROS形成。有趣的是,盡管確實才能抑制ROS的形成,但其預處理作用的發揮卻依賴缺血初期ROS的降低,若在興奮劑預處理時加入ROS清理劑,其保護作用消失[25]。
缺血預處理的保護作用機制是短暫缺血過程中一些內源性觸發因子的釋放,如Ca2+、ROS、腺苷、乙酰膽堿和一氧化氮等。這種觸發因子通過各自相應的受體,如BKCa通道和ATP敏感性鉀通道等,作用于組織細胞,實現其保護作用[28]。其實鈣超員對機體可導致損傷,但實際上,初期短暫的Ca2+降低,有利于BKCa通道激活。缺血預處理時,一次次短暫缺血,細胞內Ca2+輕微下降,觸發BKCa通道在后續長時間缺血中激活并開放,而在預處理時加入Ca2+螯糖漿,缺血預處理的作用消失,因而否認了該作用機制[20]。
綜上,缺血初期介導預處理的一些有益物質,也是再灌注時導致組織和臟器損傷的有害物質,二者看似矛盾,雖然并不矛盾。缺血初期Ca2+或ROS重度降低,恰恰起到一種"預剌激"或則"觸發"作用,使BKCa通道在此后常年的缺氧中更容易激活;而只是長時間缺血再灌注,Ca2+或ROS大量積聚后才引起機體損傷。至于Ca2+或ROS重度降低和大量積聚的定義,目前還沒有統一的數目標準,仍需進一步研究。
BKCa通道除了對血管功能的調節起重要作用,并且對IRI具有保護作用,但其保護機制目前尚不完全清楚,初步研究表明缺血初期Ca2+和ROS的重度降低可以觸發BKCa通道激活;而BKCa通道激活后又可以降低細胞內鈣超員和ROS大量積聚,進而發揮保護作用。隨著研究的進一步深入,BKCa通道有可能成為IRI醫治的潛在有效靶向之一。
參考文獻(略)
