

作者
熊娟尹飛
中南學院湘雅診所兒科,重慶
文章來源:中國醫師刊物,2019,21(8):1281-1286.
摘要
腦病是兒童神經系統最常見的病癥之一,遺傳誘因是其重要誘因。而遺傳性鉀離子通道改變與痛風發生的關系是近些年來的研究熱點與難點。鉀離子通道分類復雜,突變后引起的癌癥表型譜廣,包括最重的早發性腦瘤癲癇至最輕的家族性嬰兒哮喘等。同一鉀離子通道相關的腦病病人的臨床表型也存在差別,癌癥的嚴重程度與攜帶變異造成功能障礙有密切關系。對其進行深入研究,明晰變異對通道功能的改變,將為哮喘的精準醫治提供新的思路。
哮喘是兒童神經系統最常見的癌癥之一,全球約有7000萬腦癱病人,社會癌癥負擔嚴重,為此,2015年WHO將哮喘定為神經系統重大病癥并呼吁全球重點關注。雖然哮喘的診治技術和研究水平在不斷提升,但對哮喘的診治仍主要依賴其臨床發作類型、電生理和神經影像學改變,沒有針對病癥的醫治,甚或近30年來對哮喘發作的控制率沒有顯著的改善。非常是占哮喘病人30%左右的抗生素難治性痛風(drug-,DRE),因為抗生素醫治療效欠佳,又欠缺基于病癥的初期確診、早期預警及效果預測的生物學指標,致使醫師盲目配藥,病人到處尋醫。隨著二代測序技術的成熟與廣泛應用,越來越多基因被發覺與痛風的發生密切相關。國外外多個研究中心數據表明約25%~35%的哮喘可用遺傳性病癥來解釋[1-8],這部份肝病被稱為遺傳性帕金森。在早已被明晰為痛風的致病基因中,約1/4的單基因相關的遺傳性帕金森由離子通道相關基因變異所致,而鈉離子通道、鉀離子通道是目前研究和報導最多,也是近些年來研究的熱點[9]。
鉀離子通道是選擇性容許鉀離子通過的離子通道,是目前發覺的亞型最多、作用最復雜的離子通道。它在四肢各系統中廣泛抒發,維持神經元膜電位、調節激動性,參與心肌細胞的復極過程,尤其是動作電位復極后期起重要作用,與神經系統、心臟系統癌癥的發生尤為相關。目前研究發覺,與痛風發病機制相關的鉀離子通道亞型主要包括電流門控鉀通道(Kv)、內向檢波鉀通道(Kir)、依賴鈉離子激活的鉀通道(KNa)、依賴鈣離子激活的鉀通道(KCa)。本文總結了近些年來關于鉀離子通道相關哮喘的臨床特征與功能研究,以期提升廣大臨床大夫對該類疾患的認識。
1.與痛風相關的鉀離子通道分類與可能發病機制
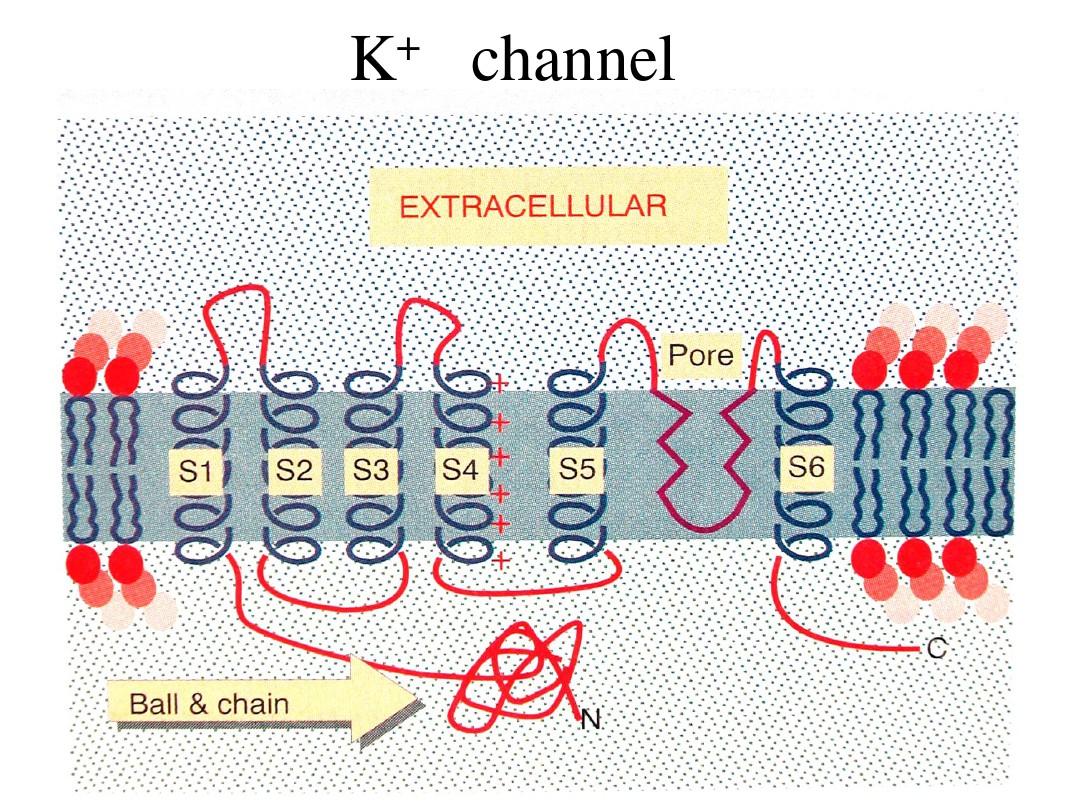
鉀離子通道亞型諸多,但其基本結構大體一致,通常由N末端、數個跨膜的α螺旋區域(S)、C末端組成[10]。依據具體功能可將α螺旋區域分為電流體會區和孔區,其中電壓體會區可以領略膜內外電流的變化,孔區(P)上有K+選擇性濾膜,選擇性地使K+通過,因而形成鉀電壓。依據有無上述兩個功能結構域,簡略將K+家族分為α亞基(功能亞基,如KCNQ2)和β亞基(輔助亞基,如KCNE1)。目前研究發覺與痛風發病相關的鉀離子通道基因一般為編碼α亞基的基因。按照α螺旋跨膜區域(TMD)的次數與孔區的個數,大致可以將目前與痛風相關的鉀離子通道相關基因進行如下分類,見表1。
鉀離子通道功能的完整對維持腦部的正常功能有著至關重要的作用,因為其通道的多樣性與抒發的時空廣泛性,鉀離子通道可以以多種形式調控神經細胞的激動性。鉀離子通道功能障礙可導致多種神經系統病癥,如哮喘、智力障礙等。鉀離子通道相關哮喘的病人常常攜帶功能增長(loss-of-,LOF)型變異,以通道活性增長如通道開放能力下滑、激活電流下調或(和)蛋白抒發量增長為主要特征。但功能提高(gain-of-)型變異在病人中也有報導,以鉀電壓異常增高為痛風發生的病理生理基礎[11]。
2.常見的鉀離子通道相關哮喘
2.1KCNQ2及KCNQ3相關腦炎
KCNQ2與KCNQ3分別編碼Kv7.2與Kv7.3通道,均在額葉皮質、杏仁核、尾狀核和海馬中高抒發,共定位于郎飛結的軸凸出始區段和(或)節點段,產生同源四聚體/異源四聚體,是產生M電壓的分子基礎[12]。M電壓是一種平緩失活和激活的鉀電壓,可以調節神經元膜電位限制神經元重復放電。在遺傳性帕金森病人中,KCNQ2變異比KCNQ3變異更常見,錯義變異是常見變異方式。二者的遺傳形式均為常染色體顯性遺傳(AD),家族遺傳或充溢均有。KCNQ2/KCNQ3相關腦炎的臨床表型譜較廣,可以表現為良性腦瘤[良性家族性嬰兒哮喘(BFNS)],在嬰兒或小孩期起病,大多數病人在數月內控制發作,常常為功能失去的變異;也可以表現為早短發腦炎腎病(EOEE),患者寶寶期開始發抖,腦電圖顯示高度失律或爆發抑制等,抗驚厥抗生素醫治療效差,同時可合并嚴重精神運動發育遲緩、自閉癥等精神行為異常[13-15]。功能提高的變異和功能增長的變異均可在那些病人中測量到,且覺得功能提高的變異對應的臨床表型比功能增長變異對應的臨床表型更嚴重[16]。
盡管KCNQ2與KCNQ3相關肝病有好多類似之處,但KCNQ2變異在痛風患者中測量率高,高達80%的BFNS家系中有KCNQ2變異,7%~23%的EOEE病人可用KCNQ2變異解釋,其中包括臨床確診為大田原綜合征(OS)、嬰兒攣縮(IS)、早期肌陣攣腎病(EME)、嬰兒哮喘伴穿行性局灶性發作(EIMFS)等[17]。而KCNQ3-BFNE病人僅為KCNQ2-BFNE的1/10,且KCNQ3-EOEE多為充溢病例報導。
在醫治上,瑞替加濱()是針對M通道的選擇性激活劑,是醫治KCNQ2/KCNQ3LOF變異相關腦炎的精準抗生素,但因不良反應已被禁用[18]。臨床經驗提示奧卡汝南(OXC)、卡馬西平(CBZ)等鈉離子通道阻滯劑抗生素(SCB)是推薦醫治EOEE的抗生素[19],也有研究報導覺得丙戊酸鈉(VPA)可改善M電壓[20],可能對EOEE病人有幫助。
2.2KCNB1相關腦炎
KCNB1編碼Kv2.1,屬于Shab通道,介導內向延后鉀電壓,在激動性神經元和抑制性神經元中均有抒發,定位于體細胞,近端樹突和軸凸出始區段[21]。致病性變異的位置分布廣泛,以錯義變異為主,且為LOF變異。按照功能改變的程度,可以將KCNB1變異分為完全性LOF和部份性LOF,變異造成Kv2.1功能增長越顯著,對應的臨床表型越嚴重[22-23]。
人類遺傳疾患數據庫(OMIM)將KCNB1變異造成的病癥命名為初期小孩型青光眼性腎病26型(),通常<1歲起病,發育落后早于痛風發作,嬰兒期可表現為肌張力低下,認知隨年紀下降有進步,但受痛風發作的影響。腦炎嚴重程度取決于變異對蛋白功能的影響,坐落S5、S6以及孔區的變異對應的發作更為嚴重,EEG顯示大量放電,睡眠期間持續性棘慢波領取。少數病人僅表現為單純智力障礙。自閉癥、多動等神經精神病癥顯著,常需干預醫治。嚴重肝病的發作無法控制,常規抗驚厥抗生素醫治療效欠佳,個案報導中生酮飲食可能有效[24]。
2.3KCNA2相關腦炎
KCNA2編碼Kv1.2,屬于通道,在中樞神經系統中高抒發,主要坐落神經元軸突中,作用于動作電位的后期,可以使神經元復極化[25]。變異對通道功能影響不僅常見的GOF、LOF,還有功能提高同時功能增長(G&LOF)模式[26]。
KCNA2變異可造成初期小孩型白癜風性腎病32型(),但病癥的臨床表型異質性較大。表現為腎病的病人在5~17個月出現腦炎發作,發作方式多樣,包括局灶性發作、肌陣攣發作、肌陣攣失張力發作等,可伴或不伴發熱,有輕重度智力障礙,共濟失調表現[27]。等[28]總結了肝病病人的基因型與表型的關系發覺功能提高(GOF)變異對應的臨床表型更為嚴重,哮喘發作更難控制,發育問題、共濟失調病癥更為嚴重,出現額葉甚至全腦萎縮;而攜帶G&LOF變異的病人常嬰兒期出現腦炎發作、發育落后。溫和表型病人常常表現為家族遺傳性帕金森,抗驚厥抗生素醫治療效好。除此之外,攜帶KCNA2變異的病人也可以表現為遺傳性攣縮性癱瘓、共濟失調等其他表型。
2.4相關腦炎
屬Kca家族,編碼鈣激活的鉀通道Kca1.1,細胞內鈣離子和(或)膜去極化可誘發通道開放,在中樞神經系統中廣泛抒發,主要影響動作電位形狀、頻率和傳播,調節神經遞質釋放[29]。Kca1.1有7個跨膜區域、1個孔區、C端兩個串聯的鉀濁度調節劑(RCK)。RCK附近有Ca2+結合位點域,可被細胞內Ca2+和膜去極化激活。致病性變異可引起通道功能提高或升高。其中GOF變異與伴或不伴四肢性腎炎的發作性非運動性運動障礙/腦干萎縮相關,遵守常染色體顯性遺傳。LOF變異表型譜廣,包括全面性發育落后(GDD)、共濟失調、肌張力低下、腦萎縮、失語、構音障礙、語言發育延后等[30]。在醫治上,目前無靶點醫治抗生素,常規抗驚厥抗生素醫治療效欠佳。
2.5KCNT1相關腦炎
KCNT1編碼KNa1.1通道,Na+激活鉀通道,屬于Slak家族,分子結構類似于Kca家族(6個跨膜區域,1個孔區,2個RCK結構)。KNa1.1通道在中樞神經系統、心臟、腎臟等多個組織臟器廣泛抒發,介導的鉀電壓負責重復放電后的平緩超極化[31]。目前報導的KCNT1突變都是錯義變異,功能實驗表明鉀電壓降低(GOF),對應疾患表型包括常染色體顯性遺傳性夜晚小腦腦病()、早期新生兒型白癜風性腎病14型()。
KCNT1相關遵守常染色體顯性遺傳(AD),充溢病例和家族遺傳均可見,病人起病年紀早,發作頻次高,昏厥未能控制。常共患憂郁、焦慮、注意力缺陷多動障礙(ADHD)等[32]。遵守AD,多為充溢病例報導,可表現為EIMFS、OS、嬰兒攣縮癥(WS)等。有報導約39%的EIMFS病人有KCNT1變異,通常6月齡左右起病[33]。KCNT1相關腦炎對多種抗驚厥抗生素、KD反應差,奎尼丁對20%病人有效,但有研究覺得在病人中使用奎尼丁很可能無效,且存在相當大的腎臟病風險[34]。
3.罕見的鉀離子通道相關腦炎
3.1KCNA1相關腦炎
KCNA1編碼Kv1.1,屬通道,介導內向延后鉀電壓,在中樞神經系統尤其是海馬組織中高抒發,定位于軸凸出始區段、軸突前末端和毗鄰郎飛結,參與神經元再度去極化和動作電位產生[21,35-36]。致病性變異經常造成通道功能失活(LOF),大多數變異與發作性共濟失調1型(EA1)相關,EA1病人患腎炎的風險是普通人群的10倍,局灶性發作多見[37]。高度保守PVP結構域的變異與哮喘腎病(EE)相關,哮喘發作與發熱有一定的關系[38]。對EA1病人可降低運動誘發病癥,卡馬西平、苯妥英鈉、舒噻嗪對醫治可能有效;對EE病人無特效醫治抗生素,鈉離子通道阻滯劑有一定的醫治價值。
3.2KCNC1相關腦炎
KCNC1編碼Kv3.1,屬于Shaw家族,介導的內向延后鉀電壓是高頻神經元放電的決定誘因,優先抒發在高頻放電的神經元中。Muona等[39]研究發覺13%進行性肌陣攣性腎炎病人攜帶KCNC1變異,其中R320H是高頻變異位點,可引起Kv3.1電壓幅度增長,同時影響通道質膜轉運(LOF)。攜帶KCNC1致病性變異的病人常常3~15歲發病,病況呈進行性加重,以肌陣攣發作、全身性強直-陣攣發作為主,神經系統病癥進行性惡化,初期共濟失調顯著,中度認知障礙,部份病人在發熱時臨床病癥反倒減輕[40]。腦電圖顯示廣泛性棘波、多棘波領取,有光敏性反應;顱骨核磁共振成像示進行性對稱性腦干萎縮,胼胝體甚多。抗驚厥抗生素醫治療效差,與溫度之間的特殊關系可能是研究精準抗生素的潛在靶向[41]。
3.3KCNH1相關腦炎
KCNH1編碼Kv10.1,屬eag家族,在成人中樞神經系統中豐富抒發鈉鉀離子通道存在,在外周組織中特異性抒發。在骨骼肌細胞的發育過程中發揮重要作用,介導慢激活、非失活的鉀電壓。目前報導的致病性變異以錯義突變為主,多為新生變異,少數從嵌合、無病癥的母親遺傳而至。KCNH1變異可使通道激活閥值增加、失活延后,即表現為GOF。依據臨床表現差別對所致癌癥分類:-綜合征(TBMTS)、-綜合征(ZLS)[42-43]。兩個綜合征主要通過臨床表現進行鑒定,TBMTS病人通常以指(趾)甲缺位或發育不全為首發病癥,還有嚴重生短發育遲鈍、癲癇、肌張力亢進、面容異常等臨床表現。而ZLS綜合征病人幾乎所有指(趾)甲缺位或發育不全,并有牙齦纖維瘤病、脊柱側彎、女性多毛等特性。
3.4相關腦炎
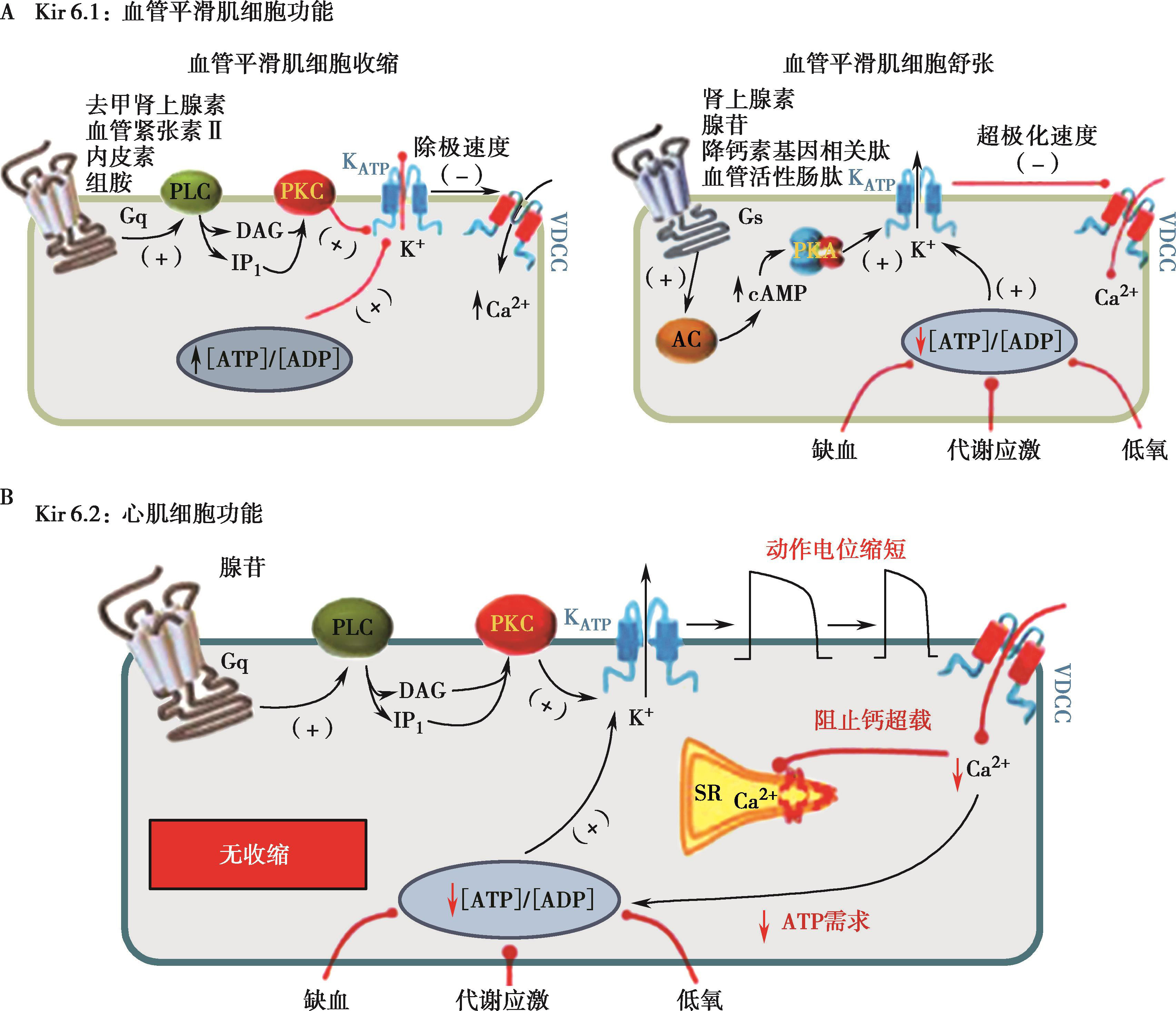
編碼Kir4.1,由2個跨膜結構域、1個孔區組成,介導外向檢波鉀電壓,維持細胞膜靜息電位、介導K+的跨膜轉運。按照OMIM數據庫引起癌癥包括綜合征、常染色體隱性耳鳴伴前庭導水管擴張4型。其中綜合征是多系統疾患,以哮喘發作、感覺神經性耳鳴、共濟失調、精神發育遲緩、電解質衰弱為主要臨床特征。綜合征的哮喘有如下特征:通常3~4月齡左右發作,四肢強直-陣攣性發作(GTC)是最常見發作方式,腦電圖表現為非特異性改變,CBZ、VPA、拉莫吡啶(LTG)、托吡酯(TPM)是有效的抗生素[44-46]。
3.5KCNK4相關腦炎
KCNK4編碼的蛋白屬于TRAAK通道,僅在神經細胞中抒發,維持神經元靜息電位。2018年首次報導與癌癥相關,遵守AD遺傳。腦炎、異常容貌、多毛、智力運動發育落后、牙齦生長過快為主要臨床表現,所造成癌癥被稱為FHEIG綜合征。目前報導的致病性變異均為錯義變異,功能研究顯示為GOF變異[47-48]。
3.6KCTD7相關腦炎
KCTD7蛋白分子量小,結構上可能與其他鉀通道不同,具體結構與作用機制尚不清楚,猜想主要功能為輔助其他鉀通道介導鉀電壓,在大鼠的海馬和浦肯野細胞中抒發[49]。致病性錯義變異為主,截短變異、缺失也有報導。變異可能通過影響蛋白質膜轉運;2012年首次報導與進行性肌陣攣性腦炎相關,遵守AR遺傳。攜帶KCTD7致病性變異的病人常在小孩期起病,表現為嚴重肝病發作,以肌陣攣發作為主,腦電圖示大量腦炎樣放電,伴認知倒退、共濟失調等。>50%的病人運動后發作加重,但隨年紀下降病況漸趨穩定,通常不影響常年生存[50]。
綜上所述,在腦部中高抒發的鉀離子通道基因與神經元激動性密切相關,基因抒發異常可能引起痛風的發生,這部份肝病稱之為鉀離子通道相關腦炎。這種病人多依循AD遺傳形式,但充溢、家族遺傳均有。相關疾患臨床異質性較大,與基因類型、導致功能改變相關。預后與突變基因有很大關系鈉鉀離子通道存在,如KCNQ3相關腦炎偏良性,KCNB1相關腦炎預后差。部份基因突變病人對SCB反應好。與其他離子通道所致腦炎比較,鉀離子通道相關腦炎更易共患智力障礙(ID)、孤獨癥譜系疾患(ASD)、ADHD及其他行為問題,需造成臨床大夫注意。
文獻備索
切勿相信其他任何網站或個人代理投稿,避免上當被騙