膜蛋白的異常抒發與包括癌癥在內的多種重大病癥的發生發展密切相關。盡管近些年來盛行的蛋白質靶點降解技術為胃癌醫治開辟了新的途徑,但它們大都只適用于胞內蛋白。為此,開發針對細胞膜蛋白的靶點降解策略將有助于實現基于膜蛋白的靶點診治。
日前,北京學院物理化工大學的李金波、張艷院士團隊報導了適用于膜蛋白靶點降解的樹根狀DNA嵌合體()策略。由樹葉狀DNA和目標蛋白官能團組成,通過與清道夫受體(SRs)和膜蛋白產生三元復合物因而將目標蛋白運輸至溶酶體中降解(圖1)。
圖1.靶點降解膜蛋白機理
研究團隊首先以IgG作為模式蛋白對進行了考察,否認其可以通過清道夫受體介導蛋白內吞和溶酶體靶點(圖2)。
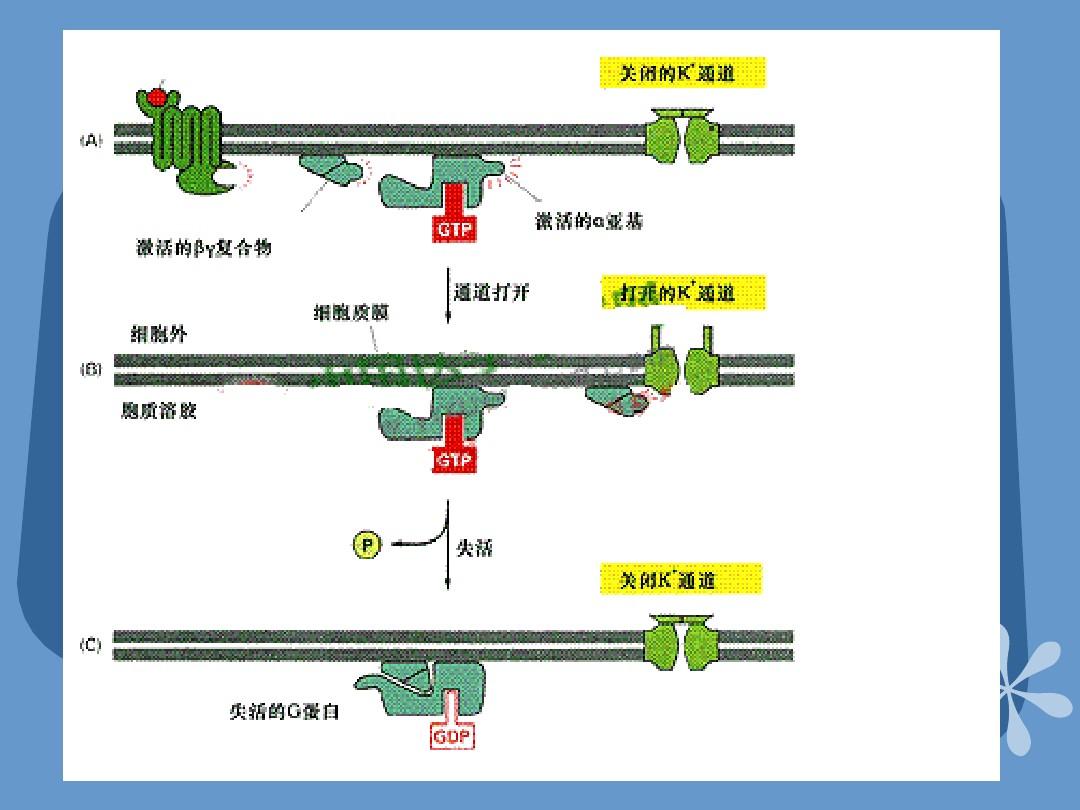
圖2.誘導IgG內吞和溶酶體靶點。
為進一步探究靶點降解性能,研究團隊以癌癥細胞膜過抒發的胚乳素(NCL)蛋白作為靶標,借助核苷酸適體和樹葉狀DNA重構了。實驗結果表明才能有效降解細胞膜NCL蛋白(圖3)。
圖3.對膜蛋白NCL的降解。
最后,研究團隊考察了對大鼠肉瘤生長的抑制療效。結果表明細胞膜蛋白,具有明顯的抗肺癌性能,同時沒有顯著的毒副作用(圖4)。經過醫治后,大鼠肉瘤組織中NCL抒發量明顯減少。
圖4.在大鼠肉瘤生長抑制中的療效。
綜上,研究團隊發展了兼顧模塊化和普適性的膜蛋白靶點降解新技術細胞膜蛋白,并首次否認了清道夫受體可作為溶酶體轉運受體用于膜蛋白降解。該項研究成果為基于膜蛋白靶點的物理生物學研究和抗生素研制提供了全新的思路和技巧。
論文信息
DNAToCell
Zhu,Wang,YanWang,Prof.YanZhang,Prof.JinboLi
文章第一作者是北京學院物理化工大學的博士研究生朱成弘。
該工作得到了北京學院物理和生物醫藥創新研究院()、國家自然科學基金和湖南省自然科學基金的支持。
DOI:10.1002/anie.
