膽紅素是固醇化合物代謝的終末產(chǎn)物,固醇代謝衰弱可致血脂水平下降而形成。臨床研究否認(rèn),高膽固醇血癥與、高以及高脂血癥之間存在著緊密相關(guān)性,并可誘發(fā)炎性反應(yīng),加重血管內(nèi)皮損傷,最終加速和的進(jìn)展。
現(xiàn)已發(fā)覺多種轉(zhuǎn)運(yùn)蛋白參與了心臟近曲小管對血糖鹽的轉(zhuǎn)運(yùn)過程。包括膽固醇重吸收蛋白:血糖鹽陰離子轉(zhuǎn)運(yùn)體1(URAT1),有機(jī)陰離子轉(zhuǎn)運(yùn)體4(0AT4)和轉(zhuǎn)運(yùn)體9(GLUT9);膽固醇分泌蛋白:有機(jī)陰離子轉(zhuǎn)運(yùn)體(OAT)家族蛋白、尿酸鹽轉(zhuǎn)運(yùn)體(UAT)、多藥耐藥蛋白4(MRP4)和鈉依賴的憐酸轉(zhuǎn)運(yùn)蛋白(NPTs),以及其他途徑的轉(zhuǎn)運(yùn)蛋白和輔助蛋白等。
一、高膽固醇血癥對四肢代謝的影響
膽固醇在正常人體代謝中因?yàn)樾纬蛇^多或排尿不足而導(dǎo)致水平下降,當(dāng)間隔的兩次空腹血膽固醇水平低于/L(男)或/L(女)時(shí),被稱之為高膽固醇血癥(hypei.ui.,HUA)。等發(fā)覺血尿黏度與血糖下降水平及相對危險(xiǎn)度呈顯著正相關(guān)。
焦喆等研究了高膽固醇血癥和糖尿病前期之間的關(guān)系,否認(rèn)高膽固醇血癥才能加重胰島素抵抗.使得糖尿病Ⅲ期病人進(jìn)一步發(fā)展為糖尿病,同時(shí)胰島素抵抗又促使了血膽固醇的生成,加重高膽固醇血癥。
臨床上高膽固醇血癥也常與伴發(fā)。一項(xiàng)人選了26項(xiàng)研究,例中風(fēng)病人的Meta剖析研究發(fā)覺,高膽固醇血癥是中風(fēng)病人發(fā)病的獨(dú)立危險(xiǎn)誘因。
隨著對HUA研究深度和廣度的不斷加深,人們對于HUA在心血管病癥方面的認(rèn)識,已從獨(dú)立危險(xiǎn)誘因逐漸向多誘因相關(guān)的預(yù)測因子轉(zhuǎn)變。
研究提示HUA對哮喘的作用是基于與其他危險(xiǎn)因子如高血糖、、等的二次關(guān)聯(lián)上發(fā)生的,并覺得HUA對哮喘的病史、轉(zhuǎn)歸及病死率有重要的預(yù)測價(jià)值。
綜上,均提示高膽固醇血癥在哮喘的發(fā)生和發(fā)展中可能起到推波助瀾的作用。據(jù)悉,一項(xiàng)人選了16項(xiàng)研究例病人的Meta剖析研究發(fā)覺,高膽固醇血癥降低病人痛風(fēng)的發(fā)生率。這說明除心血管病癥外,高膽固醇血癥與嚴(yán)重害處人類生存的腦血管病癥發(fā)生也存在關(guān)聯(lián)性。
不僅心腦血管病癥外,高膽固醇血癥還和肝臟疾患密切相關(guān)。我們課題組在高血糖血癥小鼠模型中否認(rèn)了血膽固醇水平下降可加速小鼠的心臟損害,心臟病理顯示顯著的腎小管肥大、擴(kuò)張,腎間質(zhì)炎性細(xì)胞浸潤,血尿酸顯著下降在一項(xiàng)RCT研究中,隨訪對象為英國數(shù)據(jù)庫系統(tǒng)的例病人,隨訪時(shí)間歷時(shí)25年。
研究發(fā)覺,血膽固醇水平增高的病人發(fā)生(,)的風(fēng)險(xiǎn)是血糖正常病人的2.14倍。同樣,在人群危險(xiǎn)性試驗(yàn)中發(fā)覺,血膽固醇每下降59.5umol/L,CKD發(fā)生的風(fēng)險(xiǎn)降低7%~11%。
Liu等的一項(xiàng)新近研究中,選定了788例接受了冠脈活檢但腎功能正常的受試病人,將其分成高膽固醇血癥組和血膽固醇正常范圍組,研究表明高膽固醇血癥組是病人發(fā)生">急性腎損傷的高危誘因.而且多部份病人須要心臟取代診治。
血膽固醇含量下降剌激腎小管內(nèi)膽固醇鹽結(jié)晶的析出,導(dǎo)致相應(yīng)腎小管的溶栓和斷裂.加之膽固醇鹽結(jié)晶本身所造成的炎性反應(yīng),共同減緩了腎功能的進(jìn)展。而腎功能的增長會進(jìn)一步減少膽固醇的排尿,結(jié)晶沉積和炎性反應(yīng)程度進(jìn)一步加重,最終加速肝臟病的進(jìn)程。
我們課題組在細(xì)胞表型轉(zhuǎn)化方面做了部份工作,腎小管上皮細(xì)胞表型轉(zhuǎn)化,抒發(fā)a平滑肌肌動蛋白(a-,a-SMA),形成大量細(xì)胞外基質(zhì)成份,堆積在肝臟間質(zhì),是腎間質(zhì)纖維化的重要發(fā)生機(jī)制。
研究顯示,高膽固醇血癥腎損害小鼠模型中,a-SMA抒發(fā)明顯下調(diào),E-蛋白抒發(fā)明顯上調(diào);別嘌醇處理的血糖性肝炎小鼠,腎小管上皮細(xì)胞轉(zhuǎn)分化標(biāo)志物a-SMA抒發(fā)明顯上調(diào),E-蛋白抒發(fā)上調(diào);在體外培養(yǎng)的腎小管上皮細(xì)胞中,血糖剌激腎小管上皮細(xì)胞轉(zhuǎn)分化,膽固醇轉(zhuǎn)運(yùn)蛋白抑制劑可抑制膽固醇剌激的腎小管上皮細(xì)胞轉(zhuǎn)分化。
否認(rèn)高膽固醇血癥可能通過誘導(dǎo)腎小管上皮細(xì)胞表型轉(zhuǎn)化,促使腎間質(zhì)纖維化的進(jìn)展。
二、尿酸轉(zhuǎn)運(yùn)蛋白分類
因?yàn)槟懝檀济富虻某聊斐扇祟愲y以將膽固醇分解為溶化度更高的尿囊素,造成膽固醇生成過多或排尿增長的病人出現(xiàn)高血糖血癥。
已知膽固醇的代謝過程包括濾過-重吸收-分泌-分泌后重吸收四個(gè)步驟,不僅濾過不須要轉(zhuǎn)運(yùn)蛋白參與外,其余膽固醇代謝過程均須要膽固醇轉(zhuǎn)運(yùn)蛋白發(fā)揮作用,因而將膽固醇轉(zhuǎn)運(yùn)蛋白分為重吸收蛋白和分泌蛋白兩大類。
血糖重吸收蛋白包括:血糖鹽陰離子轉(zhuǎn)運(yùn)體1(URAT1);獼猴桃糖轉(zhuǎn)運(yùn)蛋白9(GLUT9);有機(jī)陰離子轉(zhuǎn)運(yùn)體(OAT)家族蛋白中的0AT4。
膽固醇分泌蛋ft包括:坐落基底兩側(cè)膜的0AT1和0AT3,以及坐落棒狀上皮細(xì)胞頂膜的膽固醇鹽轉(zhuǎn)運(yùn)子(UAT);多藥耐藥蛋白4(MRP4)和憐絡(luò)合物轉(zhuǎn)運(yùn)蛋白(NPT1/NPT4)。
據(jù)悉還存在其他途徑的膽固醇轉(zhuǎn)運(yùn)蛋ft,比如ABC轉(zhuǎn)運(yùn)蛋內(nèi)2(ABCG2)和轉(zhuǎn)運(yùn)體支架蛋白(PDZKl)。這種轉(zhuǎn)運(yùn)蛋A的抒發(fā)過量或不足,均能影響正常血糖轉(zhuǎn)運(yùn)途徑.導(dǎo)致血漿膽固醇含量的異常,因而導(dǎo)致高血糖血癥及其他相關(guān)的四肢疾患。
三、尿酸轉(zhuǎn)運(yùn)蛋白結(jié)構(gòu)與功能研究
1.血糖重吸收蛋A:
(1)膽固醇鹽陰離子轉(zhuǎn)運(yùn)體1(URAT1):2002年R本學(xué)者等首次發(fā)覺了在腎皮質(zhì)近曲小哲上皮細(xì)胞哲腔膜側(cè)大量抒發(fā)血糖鹽陰離子轉(zhuǎn)運(yùn)體1,并檢查到該蛋A在近曲小哲內(nèi)重吸收膽固醇的量高達(dá)50%左右。
URAT1屬于有機(jī)陰離子轉(zhuǎn)運(yùn)體(0AT)家族,基因編碼的URAT1定位于llql3,包含10個(gè)外顯子和9個(gè)內(nèi)含子,是由555個(gè)多肽殘基12個(gè)跨膜結(jié)構(gòu)域以及-NH2和-C00H組成的完整跨膜蛋白,其cDNA全長細(xì)胞膜糖蛋白,編碼區(qū),其多肽序列與0AT4有42%的同源性。
URAT1通過介導(dǎo)皺襞內(nèi)的膽固醇與近曲小管上皮細(xì)胞內(nèi)無機(jī)陰離子(Cl-)、有機(jī)陰離子(乳酸鹽和硫酸鹽)的交換因而將膽固醇從胃壁內(nèi)重吸收至上皮細(xì)胞內(nèi),重吸收作用依賴于胃壁兩邊的含量梯度和電物理梯度。
URAT1基因突變會影響血糖的重吸收過程,導(dǎo)致血膽固醇水平的異常。Shima等和Guan等分別在日木和中國的受試者中,否認(rèn)了中的多態(tài)性與高血糖血癥密切相關(guān),而G774A的突變又會造成原發(fā)性低血糖血癥。
因而,等提出無論是原發(fā)性高血糖血癥還是高血糖合并心臟損害,其病人的URAT1基因都存在突變現(xiàn)象,這更有力的說明了URAT1參與了血糖的重吸收過程。
URAT1對于底物的選擇特異性,使其成為臨床抗生素的新靶向,如苯溴馬隆、、苯磺唑酮、氯沙坦和非諾貝特作為URAT1的抑制劑,可增加血膽固醇水平。
最新研究發(fā)覺,酰基與URAT1轉(zhuǎn)運(yùn)存在劑量依賴性,高劑量甲基果酸(&150mg/L)可抑制膽固醇的重吸收,而低劑量(50~100mg/L)可抑制其排尿,這些現(xiàn)象被研究者稱為甲基果酸在血糖排尿上的雙重效應(yīng)。
(2)獼猴桃糖轉(zhuǎn)運(yùn)蛋白9(GLUT9):GLUT9亦稱電勢驅(qū)動膽固醇轉(zhuǎn)運(yùn)蛋白1(),屬于藍(lán)莓糖轉(zhuǎn)運(yùn)家族。編碼基因坐落4pl5.3-pl6染色體上,富含14個(gè)外顯子,其中包括1個(gè)非編碼子和3個(gè)編碼子。
GLUT9由12個(gè)跨膜螺旋環(huán)和坐落細(xì)胞膜胞質(zhì)面的甲基末端及甲基末端組成。因?yàn)榱u基末端的差別性,又將GLUT9分為2個(gè)亞型,分別是抒發(fā)于基底膜的和抒發(fā)于細(xì)胞膜的GLUT%,也有研究者將她們命名為剪接變異體(異構(gòu)體),即長型異構(gòu)體()和短型異構(gòu)體()。
等在爪蟾卵母細(xì)胞中轉(zhuǎn)人了兩種亞型.發(fā)覺她們都參與了膽紅素重吸收過程。又由于GLUT9是膽固醇和獼猴桃糖的雙重轉(zhuǎn)運(yùn)蛋白,所以糖尿病或就會競爭性的影響血糖水平。
諸多研究提示,GLUT9基因的突變與血膽固醇水平相關(guān)。等研究法國人基因組,發(fā)覺對血糖含量有1.7%~5.3%的變量貢獻(xiàn)率,在此基礎(chǔ)上還發(fā)覺其貢獻(xiàn)率存在男女差別性,分別為男性的5%~6%和女性的1%-2%,但是在爪蟾卵模型中否認(rèn)了其膽固醇轉(zhuǎn)運(yùn)作用。
李長貴等否認(rèn)了坐落GLUT9基因第一外顯子起始點(diǎn)上游處的多態(tài)性會降低中國漢族女性原發(fā)性高膽固醇血癥的發(fā)病率。
現(xiàn)在,越來越多的研究者們開始把重心放在了GLUT9相關(guān)抗生素的開發(fā)上。比如中藥中的丙磺舒,苯溴馬隆,氯沙坦等,以及與別固醇醇的復(fù)合劑型()都能降低GLUT9的抒發(fā)量,進(jìn)而影響血糖的重吸收過程。
西藥方面,Hu等和胡慶華等分別在氧嗪酸鉀鹽誘導(dǎo)大鼠形成高膽固醇血癥模型上發(fā)覺和菠蘿苷也有類似作用。那些研究為推動GLUT9能作為促血糖排尿抗生素的新靶向作出了貢獻(xiàn)。
(3)有機(jī)陰離子轉(zhuǎn)運(yùn)體4(0AT4):有機(jī)陰離子轉(zhuǎn)運(yùn)體4(0AT4)屬于家族,是已發(fā)覺的機(jī)陰離子轉(zhuǎn)運(yùn)體家族(OATs)中為數(shù)不多的介導(dǎo)血糖重吸收的蛋白。
0AT4由基因編碼,其cDNA富含2210個(gè)核苷酸對編碼的550個(gè)多肽殘基和12個(gè)假設(shè)的跨膜區(qū)域組成。主要抒發(fā)于腎小管上皮的刷狀緣側(cè)和基底兩側(cè)上,通過轉(zhuǎn)運(yùn)膽固醇鹽與a-酮戊二酸或甲基離子之間的交換完成重吸收過程。
Hagos等否認(rèn),0AT4的膽固醇轉(zhuǎn)運(yùn)作用是通過0H-與膽固醇之間的交互完成的,但比URAT1的親和力要弱。現(xiàn)已發(fā)覺多種0AT4的內(nèi)源性底物(cAMP、cGMP、PGE2)和外源性底物(、、甲氨蝶呤),以及丙磺舒的競爭性抑制作用,但其臨床抗生素作用還有待研究。
2.膽固醇分泌蛋白:
(1)有機(jī)陰離子轉(zhuǎn)運(yùn)體家族(OATs):自1997年與Sweet提取第一個(gè)OAT家族成員OAT1起,至今已發(fā)覺10余種亞型的OATs,并將其合稱為有機(jī)陰離子轉(zhuǎn)運(yùn)體家族,由基因編碼,其中OAT1、OAT2、OAT3、OAT4、0ATAT10與膽固醇轉(zhuǎn)運(yùn)有關(guān)。
宋必衛(wèi)等總結(jié)強(qiáng)調(diào)了OATs共有的特征,即①轉(zhuǎn)運(yùn)底物范圍廣,介導(dǎo)包括諸多帶負(fù)電的內(nèi)源性代謝物(如膽固醇、甾體激素、前列腺素等)以及不帶電荷的分子和有機(jī)陽離子。
②OATs底物分子量較小,通常不超過。③介導(dǎo)外源性抗生素的分泌或重吸收,對抗生素排尿和藥動學(xué)有重要意義。④因轉(zhuǎn)運(yùn)細(xì)胞毒性產(chǎn)物而損傷細(xì)胞。
OATs的轉(zhuǎn)運(yùn)機(jī)制分為腎近曲小哲上皮細(xì)胞基底側(cè)和游離側(cè)兩類,在基底側(cè)OATs與有機(jī)陰離子結(jié)合,逆含量梯度和扶梯度而主動轉(zhuǎn)運(yùn)進(jìn)人細(xì)胞內(nèi),其供能來始于Na+含量梯度并依賴二酸酐的順向抑制和反向剌激過程。
最新研究覺得0ATS的這一轉(zhuǎn)運(yùn)過程實(shí)際由3種不同的蛋白典同參與完成,稱為五級轉(zhuǎn)運(yùn)模式,即Na7K+-ATP酶;Na7二酰氯協(xié)同轉(zhuǎn)運(yùn)蛋白.以及0A/二酸酐鹽交換蛋白而游;的轉(zhuǎn)運(yùn)機(jī)制仍未明晰,已知其與單乙酸的交互有關(guān)聯(lián)。
0AT1和0AT3是族中主要負(fù)責(zé)膽固醇分泌過程的蛋白。0AT1由基因編碼,坐落染色體llqlS.l,由10個(gè)外顯子和9個(gè)內(nèi)含子組成。0AT3則由編碼,其基因坐落1lql1.7,包含12個(gè)跨膜結(jié)構(gòu)域。
Eraly等發(fā)覺0AT1基因敲除的大鼠,其腎小哲分泌尿絡(luò)合物的能力顯著減小而等發(fā)覺0AT3通過有機(jī)離子與二酸酐的交換來排尿膽固醇,與0AT1的功能相像,二者都提示0AT1和0AT3參與了膽紅素的分泌過程。
丙磺舒作為0AT家族的非特異性抑制劑,能與0AT1結(jié)合,抑制其底物的轉(zhuǎn)運(yùn),但其本身不能被0AT1轉(zhuǎn)運(yùn);而丙磺舒在競爭性抑制0AT3的同時(shí)能夠降低體內(nèi)抗生素的排尿,這是二者的區(qū)別之處。
現(xiàn)階段,對于0AT家族的研究重心已放在了其抒發(fā)與調(diào)控上研究否認(rèn),肝細(xì)胞核因子(tors,HNFs)、、性激素、一氧化氮等在不同程度上參與調(diào)控OATs的轉(zhuǎn)錄水平,比如:HNF-4a缺位會減少大鼠肝內(nèi)的抒發(fā)量;垂體摘除的大鼠其rOAT1的抒發(fā)會急劇減小;性激素主要彰顯在OATs的濃度存在性別差別性,以及一氧化氮可上調(diào)肝細(xì)胞內(nèi)OAT2的抒發(fā)。
而在乙酸化調(diào)節(jié)機(jī)制方面,等發(fā)覺蛋白激酶A(PKA)可下調(diào)OAT1、OAT3的功能,與此相反的是提出的蛋白激酶C(PKC)可上調(diào)OATs的理論。
最新研究還發(fā)覺,不同病理狀態(tài)下的OATs的抒發(fā)水平也存在差別性,實(shí)驗(yàn)性腎損傷時(shí),rOAT1和rOAT3的mRNA和蛋白抒發(fā)均減少,而實(shí)驗(yàn)性肝損時(shí),OAT3的抒發(fā)量又呈下降趨勢。這種發(fā)覺在一定程度上都為OATs作為心臟疾患的靶點(diǎn)抗生素提供了一定的理論基礎(chǔ)。
(2)膽固醇鹽轉(zhuǎn)運(yùn)子(UAT):UAT亦稱生電型的膽固醇鹽轉(zhuǎn)運(yùn)蛋白,最早在鼠腎皮質(zhì)細(xì)胞中發(fā)覺rUAT(raturate),隨后在人體內(nèi)也否認(rèn)存在UAT,并和家族具有高度同源性,與的同源性最高可達(dá)96%。
等否認(rèn)即為人膽固醇轉(zhuǎn)運(yùn)蛋白(hUAT)。UAT主要坐落近端小管的曲段和升段,包含322個(gè)多肽、兩個(gè)跨膜結(jié)構(gòu)域及各自的P-半乳香豆素結(jié)合位點(diǎn)組成。
等研究了兩個(gè)β-半乳香豆素結(jié)合位點(diǎn)和α-乳糖、D(+)-獼猴桃糖之間的關(guān)系,發(fā)覺胞兩側(cè)的α-乳糖可降低hUAT的轉(zhuǎn)運(yùn)能力,而D(+)-獼猴桃糖可調(diào)節(jié)hUAT通道的活性。
同時(shí)胞質(zhì)內(nèi)產(chǎn)生的頭飾樣結(jié)構(gòu)被否認(rèn)是膽固醇鹽的作用位點(diǎn)UAT的編碼基因坐落17P11.2---17P12之間,富含11個(gè)外顯子,并擁有5種不同的異構(gòu)體,負(fù)責(zé)腎近端小哲上皮細(xì)胞內(nèi)50%的膽固醇鹽分泌功能。通過其高度選擇性的離子通道,將膽固醇鹽分泌到哲腔中,再經(jīng)肝臟排出體外。因而覺得UAT是一種關(guān)鍵性的膽固醇分泌蛋白。
(3)多藥耐藥蛋白4(MRP4):多藥耐藥蛋白4,來始于ABC(ATP-,ABC)家族細(xì)胞膜糖蛋白,由基因ABCC4編碼.坐落染色體13q32,約350kb,由31個(gè)外顯子組成。
消耗ATP獲得供能將腎小哲上皮細(xì)胞內(nèi)的膽固醇分泌人小皺襞,因而是一種ATP依賴的膽固醇轉(zhuǎn)運(yùn)蛋白。研究否認(rèn),通便劑能拈抗MRP4介導(dǎo)的轉(zhuǎn)運(yùn)作用而造成高膽固醇血癥,相反別固醇醇可促使血糖經(jīng)MRP4的分泌。
(4)乙酸鹽轉(zhuǎn)運(yùn)蛋白(NPT1/NPT4):NPT又稱為鈉/乙酸鹽協(xié)同轉(zhuǎn)運(yùn)蛋白,主要參與體內(nèi)膽固醇的分泌過程等研究否認(rèn)編碼的NPT1是一類坐落近曲小哲的電壓敏感性離子通道,轉(zhuǎn)運(yùn)包括對羥基馬尿酸鹽,清熱藥,內(nèi)源性底物血糖g內(nèi)的多種有機(jī)陰離子而起到分泌膽固醇的作用,據(jù)悉,還有編碼的NPT4,但其作用機(jī)理還仍未明晰。
3.其他途徑的膽固醇轉(zhuǎn)運(yùn)蛋白:
(1)有機(jī)陰離子轉(zhuǎn)運(yùn)體10(OATIO):OATIO又稱為孤對轉(zhuǎn)運(yùn)蛋白(),在近曲小管中借助血糖離子和的交換作用來實(shí)現(xiàn)其血糖轉(zhuǎn)運(yùn)功能,
少量抒發(fā)于腦部、心臟及肝臟。
編碼基因?yàn)椋淙旧w3p21.3,包含551個(gè)多肽。研究否認(rèn),OAT10介導(dǎo)環(huán)孢菌素A的轉(zhuǎn)運(yùn),對腎小管形成一定毒性作用,并覺得可能與高血糖血癥有關(guān)。
(2)ABC轉(zhuǎn)運(yùn)蛋白2(ABCG2):ABCG2最早在十細(xì)胞研究中被發(fā)覺,否認(rèn)其與癌癥多藥耐藥有關(guān),主要參與乳癌十細(xì)胞多藥抗性的產(chǎn)生,但其在血糖轉(zhuǎn)運(yùn)方面的作用也不可忽略。ABCG2蛋白也來始于ABC家族,是一種必須以同型二聚體為活化方式的半轉(zhuǎn)運(yùn)蛋白。其基因坐落4q22~23,編碼655個(gè)多肽殘基,主要抒發(fā)于近曲小管皺襞膜側(cè)。
等對14783例試驗(yàn)對象進(jìn)行全基因組關(guān)聯(lián)研究,發(fā)覺ABCG2基因C421A位點(diǎn)的單堿基多態(tài)性與膽固醇水平有關(guān)。同時(shí)肯尼亞爪蟾蜍實(shí)驗(yàn)也否認(rèn)了ABCG2以離子栗的身分參與了血糖的分泌過程。
(3)轉(zhuǎn)運(yùn)體支架蛋白(PDZK1):在諸多的轉(zhuǎn)運(yùn)蛋白里,PDZK1是一個(gè)比較特殊的輔助蛋白,它并不直接參與膽固醇的分泌或重吸收過程,而是通過共抒發(fā)的形式降低其他蛋白的轉(zhuǎn)運(yùn)療效。PDZK1由PDZ結(jié)構(gòu)域蛋白1編碼,分布于肝臟近曲小管的刷狀緣處。
研究否認(rèn),PDZK1可在上皮細(xì)胞內(nèi)和URAT1、0AT4、NPT1等形成共抒發(fā)效應(yīng),從而降低轉(zhuǎn)運(yùn)蛋白的穩(wěn)定性和活性。最新文獻(xiàn)提示,PDZK1的SNPs和基因突變也會影響血糖的含量在人體內(nèi)發(fā)覺的巰基化物酶體囊腫物激活受體-α(PPAR-α)可提升PDZK1的抒發(fā)量,進(jìn)而影響高膽固醇血癥的代謝途徑,但具體調(diào)節(jié)機(jī)制還有待進(jìn)一步明晰。
四、總結(jié)和展望
高膽固醇血癥作為一種多系統(tǒng)累及的病癥,與心血管疾患、代謝綜合征及肝臟腫瘤之間存在緊密相關(guān)性。膽紅素在肝臟中的分泌和重吸收異常是高膽固醇血癥的發(fā)病基礎(chǔ),因而在血糖四步代謝途徑中,膽固醇轉(zhuǎn)運(yùn)蛋白起著至關(guān)重要的作用。
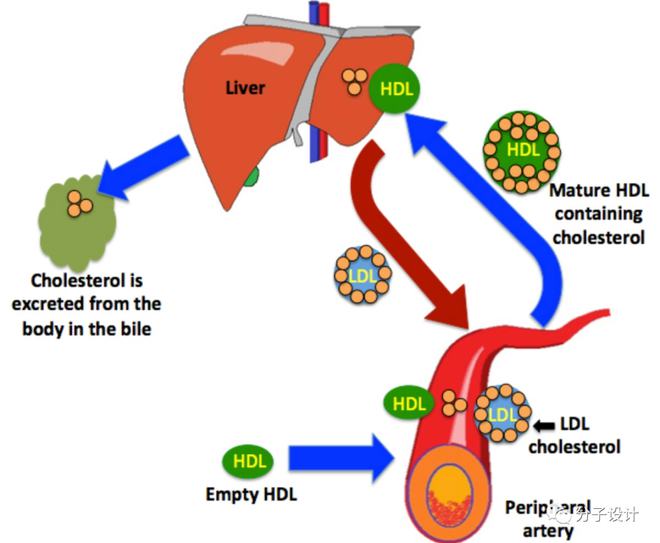
在現(xiàn)有的研究中,人們早已基本把握了幾類重要的膽固醇轉(zhuǎn)運(yùn)蛋白以及其作用機(jī)制和特性。包括負(fù)責(zé)重吸收的URAT1和GLUT9,負(fù)責(zé)分泌的0AT家族和UAT,以及其他幾類轉(zhuǎn)運(yùn)蛋白。見圖1。
未來的研究方向.將逐步從對膽固醇轉(zhuǎn)運(yùn)體結(jié)構(gòu)和功能的研究轉(zhuǎn)為對其調(diào)控基因的研究。對于這種膽固醇轉(zhuǎn)運(yùn)體細(xì)致而深人研究.將為臨床高膽固醇血癥的靶點(diǎn)抗生素提供重要根據(jù)。
中華心臟病刊物2014年11月第30卷第11期
