來源|鐵死亡club
鐵元素除了是血紅蛋白、肌紅蛋白合成的主要原料,也是多種氧化還原酶類的輔因子。作為人體濃度最多的必需微量元素,鐵穩態代謝對維持生命健康至關重要。原發性遺傳性暗紅病是鐵過載人類遺傳病,主要由HFE、HJV、TfR2、HAMP或FPN等鐵代謝調控基因突變引起多臟器鐵積聚,多累及損傷腎臟、肝臟和腎臟等重要器官,病人晚期多并發腎臟病、肝硬化或糖尿病等病癥,嚴重害處機體健康。
鐵泵蛋白(FPN)是迄今為止惟一已知的細胞鐵離子外排蛋白,它在十二指腸上皮細胞、小腸樹突狀細胞、巨噬細胞以及肝實質細胞中高抒發,其中小腸上皮細胞和巨噬細胞抒發最為豐富;FPN通過控制鐵離子的吸收、再循環和存儲來維持機體鐵穩態。課題組前期借助基因敲除大鼠在國際上首先發覺并報導了FPN在巨噬細胞以及肝實質細胞中調控鐵離子存儲和再循環的重要作用,并闡明FPN是上述組織細胞中外排鐵離子的關鍵通道蛋白。為了維持鐵離子代謝平衡進而保障細胞和組織功能細胞膜穩態劑,FPN的抒發遭到精密調控。鐵調素(HAMP基因編碼蛋白)是胰臟分泌的調控鐵穩態的核心激素,其作用靶向是FPN。當與FPN結合時,FPN降解而喪失外排鐵離子功能,從而抑制十二指腸上皮細胞的鐵吸收及巨噬細胞的鐵再循環。一旦HAMP抒發被抑制或FPN功能失調,致使鐵外排功能異常,將引起機體鐵代謝衰弱疾患。
為此,結合FPN并誘導其降解,是FPN蛋白維持鐵穩態代謝的根本機制[7]。初期研究提出,泛素化在FPN的降解過程中發揮關鍵作用。但是,結合并降解FPN的E3泛素化聯接酶至今是困惑領域的重大困局。
日前,四川學院醫大學王福俤/閔軍霞院士團隊在血液學頂尖刊物Blood(IF=17.543)在線發表了題為:ironitsE3by的研究論文,首次闡述了鐵泵蛋白(FPN)在體內外被降解的調控機制。
該研究篩選并發覺了新型E3泛素聯接酶介導了FPN的降解,于國際上率先制備了條件性敲除的大鼠模型,并首次闡明了通過調控FPN降解從而維持機體鐵穩態代謝的新機制。據悉,該研究通過轉錄組及烷基化測序的方式首次解密了DNA去乙酰化名星分子Tet1響應機體鐵衰弱,并通過表觀遺傳學調控-FPN抒發,從而控制機體對于鐵路環境的響應。
這一重磅發覺除了攻破了鐵代謝領域多年來仍未被解析的難點問題,同時為鐵衰弱相關病癥的預防提供了新靶向和新思路。
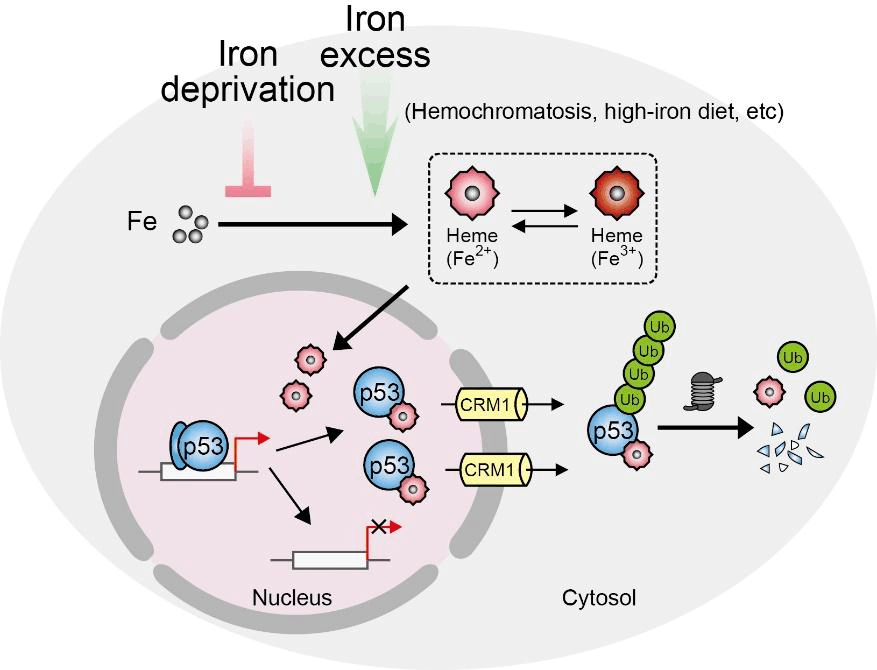
表觀遺傳修飾在調節染色質結構、調控基因抒發、維持細胞穩態等生命進程中飾演重要角色。課題組前期研究表明,表觀遺傳調控同樣參與了機體鐵穩態的維持。為了明晰機體鐵代謝衰弱過程中的關鍵表觀遺傳調控分子,該研究通過對高低鐵膳食籠養的鐵衰弱大鼠模型進行全基因組烷基化測序及轉錄組測序篩選,發覺DNA去羧基化酶Tet1參與了大鼠對于鐵路環境的響應。
Tet1參與大鼠對于鐵路剌激的響應
進一步給與Tet1敲除大鼠鐵路剌激,該大鼠出現類似暗紅病的表型細胞膜穩態劑,主要表現為血漿鐵及轉鐵蛋白飽和度下降,腎臟鐵降低,但是肝臟及小腸上皮細胞鐵離子降低的現象。通過測量鐵調素及其他鐵代謝調節基因抒發水平,研究者發覺Tet1缺位造成FPN蛋白在小腸上皮細胞及巨噬細胞積聚,從而引起大鼠鐵代謝衰弱。有趣的是,Tet1并非直接通過調控或FPN的轉錄來介導機體的鐵穩態代謝。
Tet1基因敲除大鼠鐵代謝衰弱
為了深入探究Tet1調控FPN抒發的分子機制,研究者測量大鼠原代巨噬細胞中FPN降解情況,發覺Tet1缺少造成FPN蛋白積聚、泛素化水平減小,表明Tet1通過泛素化降解路徑調控FPN抒發。但是,FPN怎樣被降解仍屬于鐵代謝領域的未知。為明晰既能促使FPN泛素化降解又能被Tet1調控的關鍵蛋白,該研究采用單向篩選的方式:借助酵母雙雜交技術在E3聯接酶文庫中篩選與FPN結合的蛋白,并進一步在喂奶植物細胞中驗證互相作用;同時在Tet1敲除體系的數據庫中篩選潛在的靶基因。通過基因疊加剖析及后續的表觀遺傳修飾剖析,研究者篩選出既能被Tet1調控,又能與FPN結合的E3聯接酶。
可能是Tet1調控的降解FPN的E3聯接酶
這么是否調控了FPN的泛素化降解呢?為了回答這一問題,研究者首先在體外檢查了對于FPN的調控作用,結果顯示外源明顯推動了蛋白酶體及溶酶體依賴的FPN的泛素化降解,功能性缺位或突變的酶活位點,該降解作用顯著被抑制。上述結果闡明了FPN是的作用靶向。
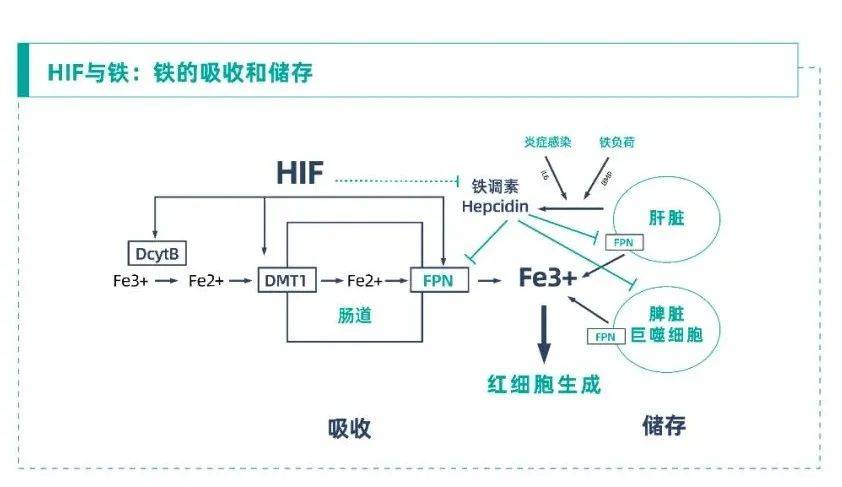
推動FPN降解
為了進一步明晰的生理功能,研究者分別建立了巨噬細胞和小腸上皮細胞特異性缺位的基因敲除大鼠(/Lysm和/)。令人驚奇的是,/Lysm和/大鼠表現出與Tet1敲除大鼠類似的對鐵路響應異常的鐵代謝衰弱表型,表明其在鐵穩態代謝調控中的重要作用。通過分離大鼠原代巨噬細胞,研究者發覺缺位造成FPN降解減小。因為是誘發FPN發生內攻占降解的重要分子,為闡明在-FPN調控軸中的關鍵作用,研究者給與/Lysm大鼠注射或激活劑LPS,結果顯示缺位明顯抑制了依賴的FPN降解。上述結果既明晰了體內在調控的FPN降解中的重要作用,同時提示有望成為-FPN相關鐵代謝衰弱疾患的醫治靶向。
巨噬細胞和小腸上皮細胞特異性敲除
其實,這項研究于國際上首次發覺并報導了調控FPN降解的E3泛素聯接酶。該成果成功制備了條件性敲除大鼠,于體內外探求并闡明了調控FPN降解及鐵穩態的分子機制;該成果提出了Tet1--FPN軸響應機體鐵路負荷的新機制,除了彌補了鐵代謝研究領域關于FPN降解調控的空白,同時為鐵代謝衰弱相關疾患的預防提供了新靶向和新策略。
Tet1--FPN調控軸模式圖
王福俤團隊博士后蔣麗和博士生王佳明為論文共同第一作者;四川學院王福俤院士、閔軍霞院長為共同通信作者。此項研究得到中國科大學生物物理與細胞生物學研究所胡榮貴研究員、浙江學院生命科學研究院金建平研究員、浙江學院醫大學孫啟明院士、浙江學院實驗植物中心洪勝輝以及醫大學公共技術平臺陳靜瑤的大力幫助。項目遭到國家重點研制計劃、國家自然科學基金以及中國博士后科學基金的經費支助。
論文鏈接:
