

免費下載!
[!--downpath--]實驗活動1氮氣的實驗室制取與性質
基礎練習
1.實驗室制取氫氣,不選用的藥品是()
A.高錳碘化鉀B.二溴化氫
C.氯碘化鉀D.空氣
2.實驗室里用排水法搜集二氧化碳,根據的二氧化碳性質是()
A.無色B.無味C.不易溶于水D.支持燃燒
3.用高錳碘化鉀制取氫氣時,發覺水槽里的水變紅了,緣由是
A.二氧化碳溶于水導致的
B.忘了在試管口處放一團棉花
C.二氧化碳與水發生了物理反應生成了藍色的物質
D.集鋼瓶沾上了少許黑色顏料
4.實驗室用高錳碘化鉀制氫氣,并用排水法搜集二氧化碳的實驗步驟是
①檢查裝置的氣密性②收集二氧化碳③停止加熱④將導管移出海面⑤開始加熱⑥連接儀器⑦固定試管⑧加入藥品
A.①⑧⑥⑦⑤②④③B.⑥①⑧⑦⑤②④③
C.①⑧⑦⑥⑤②③④D.⑥①⑧⑦⑤②③④
5.用推拉注射器活塞的方式可以檢測如圖裝置的氣密性。當平緩推動活塞時制取氧氣實驗視頻,假如該裝置氣密性良好,能觀察到
A.有液體步入注射器內B.長頸漏斗內液面上升
C.長頸漏斗管口形成氣泡D.長頸漏斗內液面高于瓶內液面
6.實驗室搜集二氧化碳,既可以選向下排空氣法又可以選排水法的緣由是
①氧氣不易溶于水②氧氣易溶于水③氧氣密度比空氣大④氧氣密度比空氣小
A.①④B.②④C.②③D.①③
7.下述有關加熱高錳碘化鉀制取氫氣實驗操作的說法中制取氧氣實驗視頻,正確的是
A.組裝裝置時,應遵守“先左后右”“先上后下”的循序
B.導管口有氣泡形成的時侯開始搜集二氧化碳
C.加熱試管時,要先預熱試管,后固定在藥品下方加熱
D.必須用燃著的鋼條檢驗是否搜集滿
8.某二氧化碳可用右圖所示方式搜集,猜想該二氧化碳一定具有的性質是()
A.密度比空氣大B.易溶于水C.無色無味D.物理性質開朗
提高練習
9.“證據推理”是物理學科核心素質的組成要素之一。如右圖,將帶火星鋼條放在集氣瓶口,鋼條復燃。由上述證據推理,不能得到的推論是
A.該二氧化碳是二氧化碳B.氫氣密度小于空氣
C.二氧化碳不易溶于水D.二氧化碳搜集滿了
10.如圖所示,將某物質放到盛有二氧化碳的集鋼瓶中燃燒,待熄滅并完全冷卻后,發覺玻璃管下邊的吝嗇球漸漸鼓上去,則該物質可能是
A.蠟燭B.紅磷C.木炭D.硫粉
11.實驗室用KMnO4制二氧化碳并驗證二氧化碳的性質,下述操作正確的是
A.檢測裝置氣密性
B.加熱KMnO4制O2
C.驗證O2已集滿
D.硫在O2中燃燒
12.右圖是實驗室加熱高錳碘化鉀制取氫氣的裝置圖,下述有關實驗操作剖析錯誤的是()
A.氣密性檢測:用手握住試管,觀察到水底導食道有氣泡冒出,說明裝置不漏水
B.試管口略向上傾斜:避免試管壁上的水流入試管頂部,造成試管炸裂
C.加熱:直接用酒精燈的火焰對準藥品所在位置加熱
D.停止加熱:先把導管移出海面,再熄滅酒精燈
13.如圖為中學物理常見二氧化碳的發生和搜集裝置,有關這種裝置用途的說法正確的是
A.裝置I、V的組合可作為實驗室借助氯碘化鉀制取氫氣的裝置
B.裝置Ⅱ、V的組合可作為實驗室制取氫氣的裝置
C.能夠選用裝置Ⅲ或IV來搜集二氧化碳,只須要考慮二氧化碳的密度
D.裝置V可以用于搜集H2、O2、NH3等二氧化碳
14.圖為實驗室用等質量的高錳碘化鉀和氯碘化鉀(另加少量鋅粉)分別制取氫氣的數據剖析示意圖。下述推論正確的是:()
A.同時開始加熱,先搜集到二氧化碳是氯碘化鉀
B.反應所用時間較長的是高錳碘化鉀
C.加入少量鋅粉使氯碘化鉀形成二氧化碳質量降低
D.加熱等質量的高錳碘化鉀和氯碘化鉀,氯碘化鉀放出二氧化碳較多
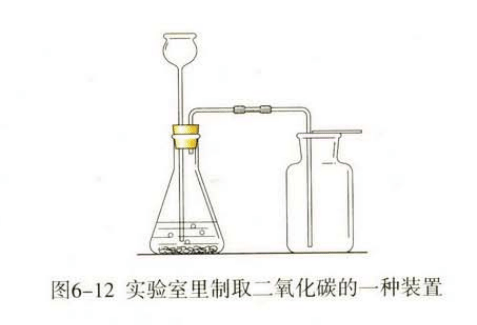
15.按照下述所示裝置,結合所學知識回答問題。
(1)用A裝置制取氫氣,反應的文字表達式是。
(2)用B裝置搜集二氧化碳,當聽到有時開始搜集;當聽到集氣瓶口有時說明已搜集滿。
(3)C裝置中飽含水時,可作為二氧化碳的搜集裝置,則二氧化碳應從(填“a”或“b”)端通入。
(4)按右圖所示,將帶火星的鋼條分別插入盛滿氫氣的集鋼瓶中,觀察到鋼條復燃,且在①中燃燒比在②中旺。以上實驗現象說明了氫氣的性質:①;②。
16.課堂討論
(1)若果某同事用排水法治得的二氧化碳不純,你覺得可能緣由有什么?
(2)把紅熱的木炭插入盛有二氧化碳的集鋼瓶時,為何要由集氣瓶口向上平緩插入?
17.物理興趣小組對二氧化碳的制取進行了如下探究。
Ⅰ、實驗室制取氫氣。
(1)寫出上圖所示裝置中標號儀器的名稱:a。
(2)實驗室中用A裝置制取氫氣,發生反應的符號表達式為;試管口棉花的作用是。
(3)搜集一瓶較為干燥的氮氣應選用的搜集裝置為(填代號),搜集滿氫氣的集鋼瓶應(填“正”或“倒”)置于桌面上,檢驗氫氣是否搜集滿的方式是。若用排水法搜集二氧化碳時,當觀察到氣泡時才開始搜集,否則搜集的二氧化碳不純。
(4)在結束實驗時應先,再,其目的是。
Ⅱ、探究影響二溴化氫氨水分解速度的誘因。實驗裝置如右圖所示(夾持儀器已略),實驗數據見下表。
實驗序號
二溴化氫堿液的含量
30%
30%
15%
30%
30%
30%
二溴化氫堿液的容積(mL)
水槽中水的體溫(℃)
20
90
70
70
20
20
錐形瓶中的物質
0.
0.
60分內形成二氧化碳(mL)
0.0
41.0
4.5
12.1
2.0
650.0
(5)實驗2中應加入胺基化氫堿液的容積x是mL。
(6)得出“過氧化氫堿液的含量越大,分解速度越大”結論所根據的實驗是(填序號)。
(7)通過實驗1、2、4對比,可得出的推論是。