

在我的記憶中,我學生時代并沒有學過內力的概念。 我只知道熱、功、熱功當量等熱學概念。 后來,人們發現功和熱本質上是同一回事。 內能的概念是基于焦耳等人大量精確的熱功當量實驗而提出的。 內能概念的確立,標志著熱力學第一定律(即能量轉換與守恒定律)的真正確立。 因此,內能的概念應該是現代物理學才有的物理概念。 許多智能系統無法識別它。 許多人不知道什么是內能,更喜歡稱之為熱能。 本文就給大家科普一下。 內能到底是什么?

本質上,物體的內能應該是物體內部所有微觀粒子運動的動能、勢能、化學能和原子核能的總和。 一般情況下,由于物質的分子結構、原子結構和核結構都比較穩定,不會輕易發生變化,因此這些能量的變化可以忽略不計,除非發生電子躍遷或化學反應。
內能的分類分為狹義內能和廣義內能。
狹義的內能。 它是不涉及電子躍遷、化學反應、核反應能的分子動能和分子勢能的總和,是物理學中的內能概念。
如果涉及電子躍遷、化學反應和核反應能,則一般稱為熱力學能,以前稱為熱能。 可見內能與什么有關,熱能和內能是有區別的。
內能最廣泛的定義是熱力學能和電子能的總和。 最廣義的內能當然是物體或系統內所有微觀粒子一切形式運動的能量總和,包括熱力學能、電子能和原子核內能的總和。 。
分子動能。 包括分子的平動能、旋轉能和振動能。 物體是由分子組成的,分子不斷地進行無規則運動,因此分子具有動能。 由于運動永遠不會停止,因此內能永遠不會為零。 由于運動是不規則、混亂的,所以存在旋轉或振動。 速度可大可小,無法準確描述其運動的快慢。 因此只能用平均速度或平均動能來描述。 溫度是分子不規則運動強度的具體表現。 溫度越高,平均動能越大,分子運動越劇烈。
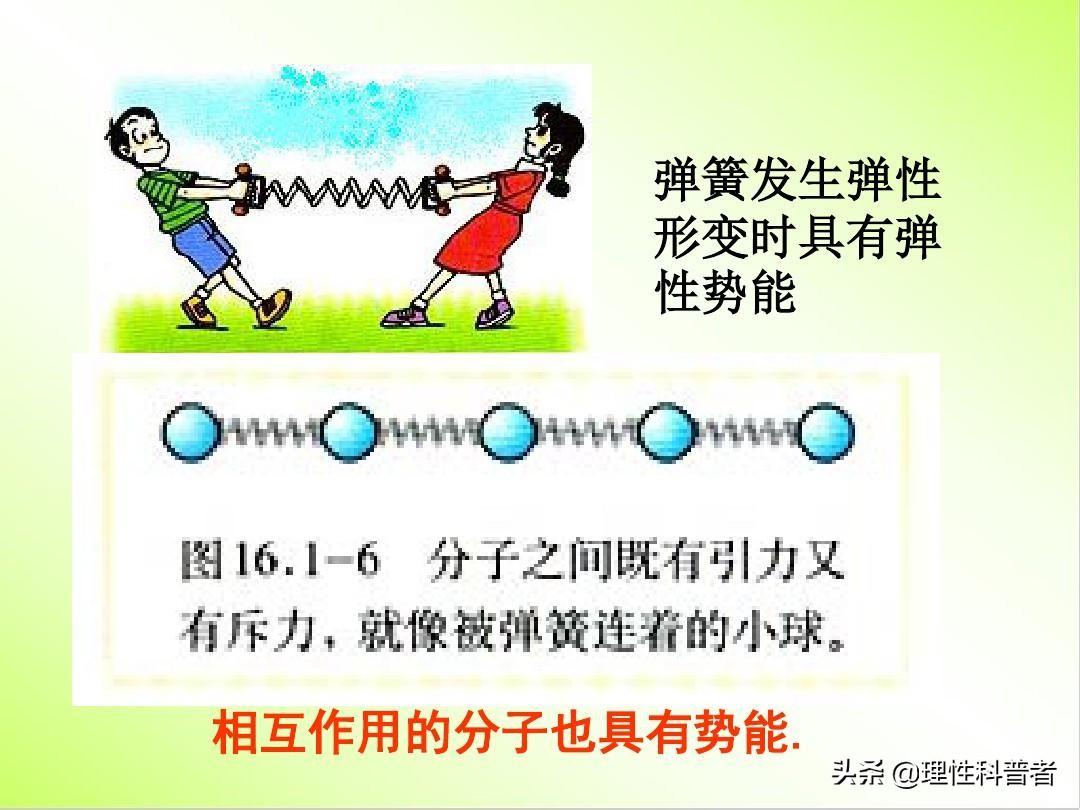
分子勢能。 吸引力和排斥力源自分子間相互作用。 分子間力也稱為范德華力(廣義分子間力還包括氫鍵力等特殊分子間力)。 一般來說,當分子距離較遠時,分子間作用力主要是引力。 隨著距離減小,重力增大。 但當距離減小到一定程度時,排斥力開始出現,引力變小,分子間力也變小。 主要表現是排斥。 巨大的斥力使分子的動能幾乎為零,全部轉化為分子勢能。 失去動能的分子在強斥力的作用下轉化為分子動能。 這就是分子的碰撞過程。
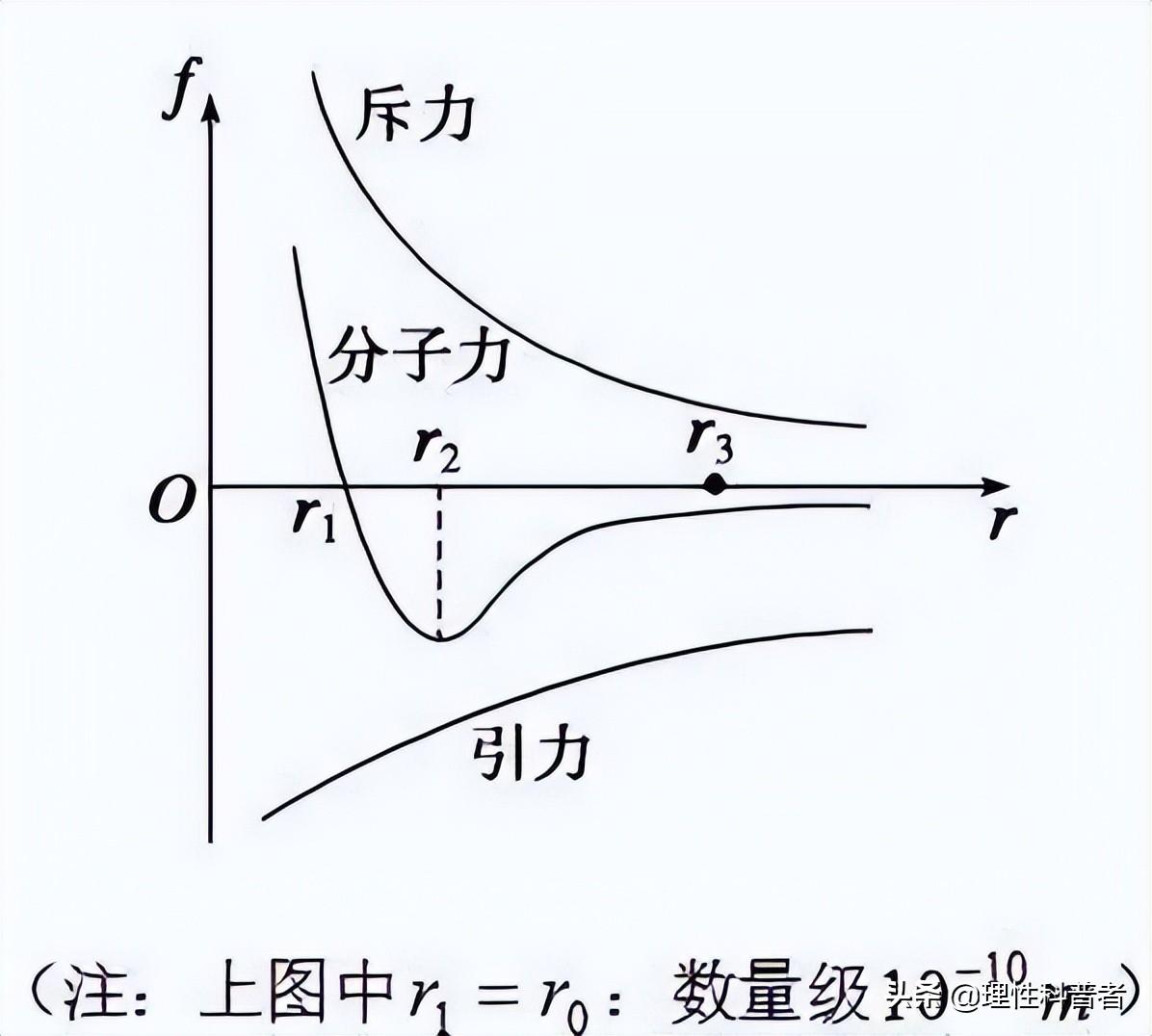
判斷分子勢能一般取決于物質的狀態。 當物質改變狀態時,分子勢能會發生突然的變化。 例如,冰的融化是一個吸熱過程。 0°C 的冰在 0°C 時融化成水。 溫度不變,分子的動能不變。 因此,吸收的熱量被用來增加分子的勢能。
由于分子是由原子核和電子組成,因此內能主要取決于電子的能量和原子核內部的能量。 原子核內部的能量不容易表達。 因此,分子內部的能量主要是電子的能量,包括電子的能量。 動能、電子和原子核的引力勢能、電子與電子之間的排斥勢能,當然還有原子核之間的排斥勢能。 其中,維持分子或原子穩定性的電子和原子核的引力勢能占主導地位。
影響內能的因素。 內能的大小與物體的溫度(影響分子的動能)、物體的質量(影響分子的數量)、構成物體的物質種類以及存在性有關物體的狀態(影響體積、影響分子間力、影響分子勢能)。 請注意,單個分子沒有內能,而物體在任何情況下都具有內能。
當我們比較物體的內能時,必須同時考慮以上因素。 不能說溫度高的物體內能就大,也不能說內能大的物體溫度就高,也不能說質量大的物體就大。內能。
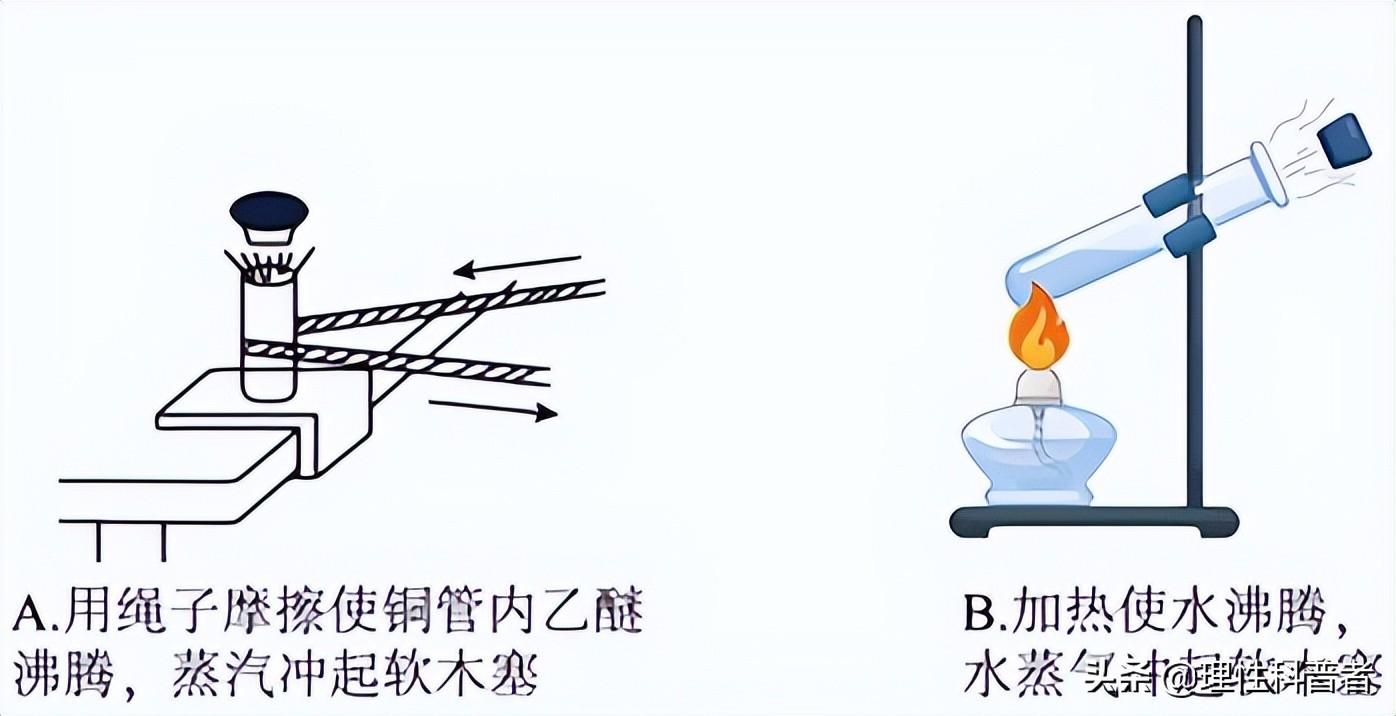
人類關心的是物體內能的變化有多大,而沒有人知道物體的內能有多少。 如何改變物體的內能? 對于特定的物體,當物體的溫度發生變化時,分子不規則運動的速度發生變化或體積發生變化,因而物體的內能發生變化。 顯然,只有傳熱和做功才能改變物體的內能。 傳熱有三種形式,即熱傳導、氣體和液體的熱對流、熱輻射。 傳熱的條件是物體之間必須存在溫差。 做功和傳熱在改變內能的作用上是等效的。 功是能量形式的變化,傳熱是物體之間內能的傳遞。
對于由定量物質組成的系統,在其他因素不變的情況下,通過做功和傳熱與外界進行能量交換內能與什么有關,引起系統內能的變化,由關系式ΔU=W+Q確定,其中ΔU是內能的變化,W是外界與系統之間所做的功,Q是系統與外界之間交換的熱量。 這是熱力學第一定律。