水是世界上最普通的,也是最反常的物質(zhì)。
撰文|瞿立健
我們這個(gè)世界有好多“怪異”的東西,例如量子、黑洞、暗物質(zhì)、暗能量、宇宙起源,等等。這種東西離我們的日常生活有點(diǎn)遠(yuǎn),不過(guò),日常生活中也有與那些東西同樣奇特的東西,那就是——水。
奇特的水
司空見慣的水在科學(xué)上卻是最奇特的液體。有科學(xué)家列出出水起碼有66種反常性質(zhì)。這種奇特的性質(zhì)里,好多彰顯在專門的科學(xué)實(shí)驗(yàn)里,也有一些性質(zhì)可以輕松表現(xiàn)下來(lái)。
把一塊冰——固態(tài)的水——扔進(jìn)冷液態(tài)水里,你會(huì)發(fā)覺,冰會(huì)浮在海面上,由于冰的密度大于液態(tài)水。這就是奇事一樁,通常液體匯聚為固體,密度減小,由于原子或分子在固體中的排列比在液體中更緊密。
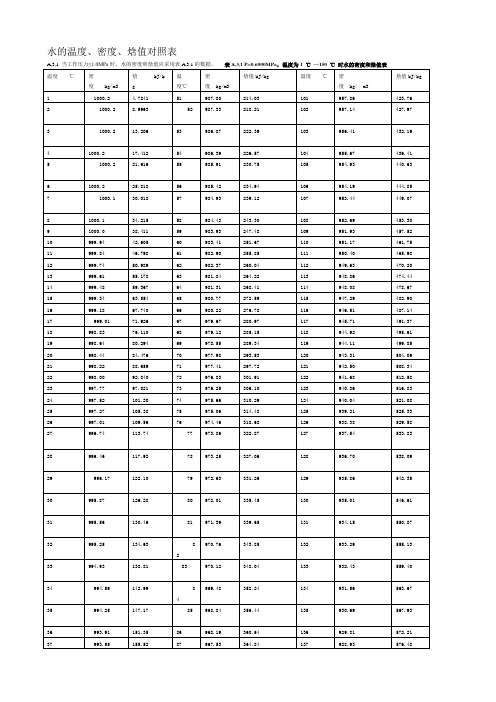
水面正在結(jié)冰的時(shí)侯,用體溫計(jì)測(cè)一下各深度處水的氣溫,海面處水溫為0℃,而湖頂部氣溫為4℃,這是由于水在4℃時(shí)密度最大。
液態(tài)水的密度小于冰,且冰點(diǎn)時(shí)其密度大于氣溫稍高時(shí)的密度,否則,河流和湖泊會(huì)從下往上結(jié)冰,水底生物將無(wú)法存活。這對(duì)生命有重要意義,更不用說(shuō)它們挺過(guò)歷史上多次漫長(zhǎng)的二疊紀(jì)。
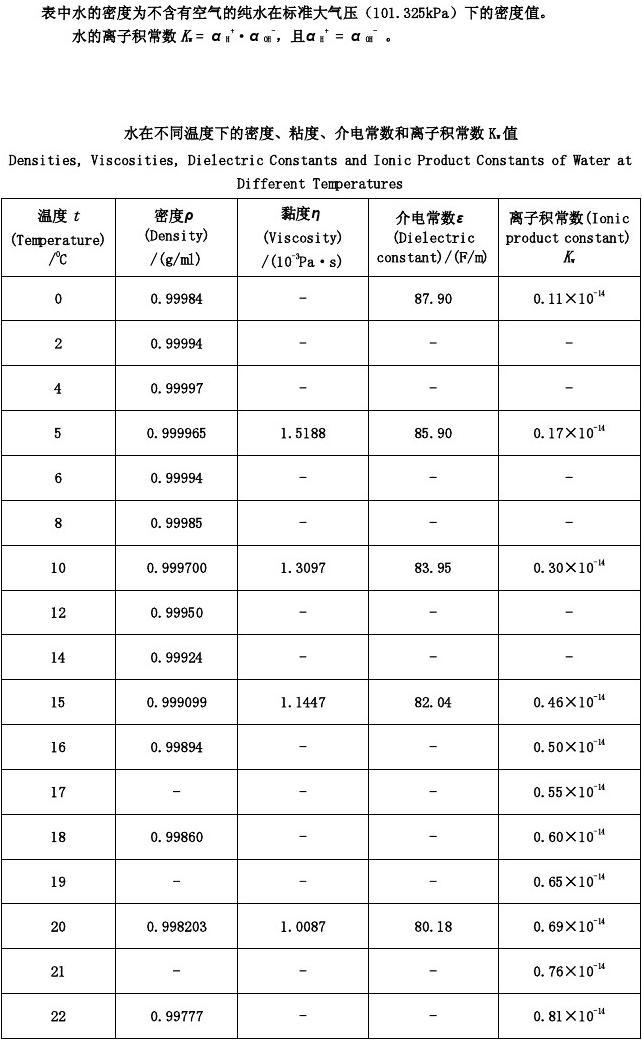
各氣溫下水的密度。圖源:CRCofand
河水頂部氣溫為4℃。圖源:~/sq//.png
另一方面,讓水下降一定濕度,須要吸收的熱比通常液體出奇得高,常下臥室的讀者都有生活經(jīng)驗(yàn),油的升溫要比水快。水放熱能力強(qiáng),這也有意義——如果放熱能力很差,氣候稍有變化,生態(tài)系統(tǒng)將遭遇滅頂之災(zāi)。
水結(jié)冰時(shí)要膨脹,冰溶化時(shí)卻收縮。水起碼能產(chǎn)生17種晶體——即冰。
本文前面會(huì)再列出幾種水的奇特性質(zhì)。
我們應(yīng)當(dāng)對(duì)水的奇特性質(zhì)有感恩之心,否則,復(fù)雜的生命似乎不會(huì)存在,我們也就沒(méi)有機(jī)會(huì)閱覽這篇文章,感受水的神奇。
水為何行為古怪?
科學(xué)家思索問(wèn)題,通常遵循還原主義思維,物質(zhì)性質(zhì)源自物質(zhì)的結(jié)構(gòu)。
這么,水是哪些樣的結(jié)構(gòu)呢?
雙水記
故事溯源至1976年。
日本普渡學(xué)院的奧斯汀·安吉爾()和羅賓·斯皮迪(Robin)將水降溫,想瞧瞧水能降到多低的氣溫。
你可能會(huì)問(wèn),減少到0℃不就結(jié)冰了嗎?
不一定,假如容器內(nèi)十分潔凈,水十分平淡,在0℃以下仍會(huì)保持液體狀態(tài),這叫“過(guò)熱水”。
一瓶過(guò)熱水遭到擾動(dòng)以后快速結(jié)冰。圖源:按照視頻制做
安吉爾和斯皮迪發(fā)覺一些奇怪的現(xiàn)象:體溫越低,過(guò)熱水的密度分布極其不均勻。常理來(lái)說(shuō),氣溫越低,水的密度應(yīng)當(dāng)越均勻。
水上面發(fā)生了哪些事情?
限于當(dāng)時(shí)的實(shí)驗(yàn)條件,難以觀測(cè)得更細(xì)致。
1992年,加拿大波士頓學(xué)院的彼得·普爾(PeterPoole)和吉恩·斯坦利(Gene)對(duì)水進(jìn)行了計(jì)算機(jī)模擬研究(1992,360,324–328),再現(xiàn)了實(shí)驗(yàn)中類似的現(xiàn)象。更重要的是,計(jì)算機(jī)模擬可以估算體系的各類性質(zhì),甚至分子的具體運(yùn)動(dòng)情況。
普爾和斯坦利依據(jù)她們的計(jì)算機(jī)模擬結(jié)果,看出過(guò)熱水的行為似乎和普通水弄成水蒸汽的情況很類似。普通水在一些特殊條件下,密度分布也會(huì)顯得極端不均勻。下邊我們先簡(jiǎn)單介紹一下水從液體變?yōu)槎趸嫉倪^(guò)程。
二氧化碳和液體的分界線——汽化線。圖源:《邊緣奇跡:相變和臨界現(xiàn)象》
如上圖所示,液體浮力保持為P0,升溫,即液體狀態(tài)按圖中線LQ聯(lián)通,抵達(dá)點(diǎn)Q時(shí),一部份液體開始?xì)饣磁啥趸肌4藭r(shí)雖然繼續(xù)加熱,但氣溫卻不再下降,而是保持在T0。直至全部液體弄成二氧化碳,氣溫才繼續(xù)沿QG下降。在各類浮力下做實(shí)驗(yàn),可以得到一系列氣液共存的點(diǎn),把這種點(diǎn)連上去,就得到一條曲線——汽化線。
仍然升溫或加壓,氣化線會(huì)仍然延展下去還是在某個(gè)點(diǎn)急遽而止?
實(shí)驗(yàn)發(fā)覺水的密度是什么它表示什么,氣化線有個(gè)終點(diǎn),這個(gè)點(diǎn)叫作臨界點(diǎn),即右圖中的點(diǎn)。
氣化線有個(gè)終點(diǎn),即臨界點(diǎn)。圖源:《邊緣奇跡:相變和臨界現(xiàn)象》
臨界點(diǎn)之外,物質(zhì)是處于氣態(tài)還是液態(tài)?
這個(gè)問(wèn)題是沒(méi)有意義的,由于臨界點(diǎn)之外,氣態(tài)和液態(tài)的差異不復(fù)存在。沿圖中實(shí)線做實(shí)驗(yàn),物質(zhì)可以從液態(tài)點(diǎn)連續(xù)地弄成氣態(tài)。
在氣固相變的臨界點(diǎn)附近,密度分布也是極端不均勻的。一個(gè)相關(guān)的實(shí)驗(yàn)現(xiàn)象是臨界乳光,如右圖所示。(編者注:可參見《臨界現(xiàn)象200華誕,是誰(shuí)最早發(fā)覺了這個(gè)化學(xué)現(xiàn)象?》)
用光照射受熱的乙酸,圖1為氣液共存狀態(tài),圖2中發(fā)生了臨界乳光現(xiàn)象,即物質(zhì)散射的光為紅色,這說(shuō)明在光的波長(zhǎng)這么小的尺度上,物質(zhì)的密度都不均勻,物質(zhì)顯得不透明且變得混濁。圖3為超臨界流體。圖源:維基百科
通常來(lái)說(shuō)物質(zhì)有氣態(tài)、液態(tài)和固態(tài)三種狀態(tài)。不過(guò),數(shù)學(xué)學(xué)中更常用的詞是“相”,而不是“態(tài)”。
物質(zhì)的“相”的種類比通常所說(shuō)的“態(tài)”的種類要多得多。也就是說(shuō),對(duì)應(yīng)于同一個(gè)態(tài),還可以有許多不同的“相”。例如,水的固態(tài)是冰,但冰有好多種不同的結(jié)晶形式,它們對(duì)應(yīng)于不同的“相”。
物質(zhì)從一種相轉(zhuǎn)換成另一種相,稱為相變。水從液態(tài)(或稱氣相)弄成氣態(tài)(或稱液相)就是一種相變。
我們回到普爾和斯坦利的實(shí)驗(yàn),她們通過(guò)計(jì)算機(jī)模擬發(fā)覺,過(guò)熱水在某氣溫附近密度也會(huì)顯得及其不均勻,這與氣固相變臨界點(diǎn)附近的情況很類似。于是,普爾和斯坦利構(gòu)想,哪里是個(gè)臨界點(diǎn),過(guò)熱水也可以發(fā)生相變,兩相分別是低密度水和萊西度水。
普爾和斯坦利的構(gòu)想得到后續(xù)更精確的水模型的模擬結(jié)果支持,顯示她們的推測(cè)很靠譜,即水不僅氣化線的臨界點(diǎn)之外,過(guò)熱水還有一個(gè)臨界點(diǎn)。
過(guò)熱水會(huì)發(fā)生高、低密度水相變,類似普通水的氣固相變。注意,本圖中縱座標(biāo)為體溫,橫座標(biāo)為浮力。圖源:World
實(shí)驗(yàn)上能不能見到這個(gè)臨界點(diǎn)呢?
很難,這個(gè)臨界點(diǎn)在-45℃,在如此低的氣溫下,水很容易就結(jié)冰了。
全世界多個(gè)杰出的課題組展開了研究,努力了26年,在2017和2018年,兩個(gè)獨(dú)立的精致實(shí)驗(yàn)(2017,358,1589;2018,359,1127)確定,第二個(gè)臨界點(diǎn)是存在的,過(guò)熱水在適當(dāng)條件下可以發(fā)生相變,即存在兩種結(jié)構(gòu)的水。
具體是哪些樣的結(jié)構(gòu)呢?
日本斯德哥爾摩學(xué)院的安德斯·尼爾松()院長(zhǎng)與其合作者在這個(gè)方面做了系統(tǒng)的工作,我們直接介紹她們所得到的推論。
一水兩構(gòu)
水的結(jié)構(gòu)是水份子之間的互相作用決定的。
水份子由兩個(gè)氫原子和一個(gè)氧原子組成,兩個(gè)氫原子分別與氧原子緊密結(jié)合在一起,產(chǎn)生V字型結(jié)構(gòu),它們之間的結(jié)合形式物理家稱之為“共價(jià)鍵”。
氧原子和氫原子通過(guò)共價(jià)鍵結(jié)合產(chǎn)生水份子。圖源:科普中國(guó)
水份子整體是電中性的,但在分子內(nèi)部,電量分布是不均勻的,氧原子頗有負(fù)電,而兩個(gè)氫原子頗有正電。當(dāng)一個(gè)水分子中的氧原子和另一個(gè)水分子中的氫原子緊靠時(shí),兩個(gè)水份子之間還會(huì)形成吸引作用,這些作用物理家稱為“氫鍵”。
水份子間官能團(tuán)的產(chǎn)生。圖源:科普中國(guó)
官能團(tuán)要比共價(jià)鍵弱得多,很容易被破壞。有人形象地說(shuō):“氫鍵相當(dāng)于兩個(gè)人手拉手,可以拉也可以分。共價(jià)鍵聯(lián)接的是你自己的手和腳,不能分開。”
尼爾松依據(jù)她們的實(shí)驗(yàn)結(jié)果,提出水分子在構(gòu)象的影響下,可以有兩種排列方法,按多面體有序排列或隨機(jī)無(wú)序排列,分別組成低密度水和萊西度水。
水有兩種結(jié)構(gòu)。圖源:New
以上理論可以解釋水的眾多反常性質(zhì),下邊略舉幾例。
正解反常
?冰的密度比水小。
冰中的水份子排列方法與低密度水底水份子排列方法相同,即多面體結(jié)構(gòu),而水底還有無(wú)序結(jié)構(gòu)的新泰度水,因而,水的平均密度小于冰的密度。
?水在4℃時(shí)密度最大。
在0°C時(shí),水份子更多地處于多面體結(jié)構(gòu)的有序相,即低密度水占優(yōu)勢(shì)。極端情況下,假如完全沒(méi)有無(wú)序的青州度水,液態(tài)水就締結(jié)冰了。氣溫下降,分子無(wú)規(guī)則的熱運(yùn)動(dòng)就越劇烈,有序結(jié)構(gòu)就越少,萊州度水越占優(yōu)勢(shì),即水的密度下降。但當(dāng)水溫達(dá)到4°C以上時(shí),分子熱運(yùn)動(dòng)使水份子寬度隨氣溫下降而減小,水的密度從而減少。
分子仍然做著無(wú)規(guī)則熱運(yùn)動(dòng),氣溫越高,分子熱運(yùn)動(dòng)越劇烈,有序結(jié)構(gòu)就越無(wú)法維持。圖源:。
?水的比熱容明顯小于絕大多數(shù)液體。
加熱物質(zhì),使其升高三定量的體溫,但水比其他液體須要熱量更高,即比熱容更大,由于水須要一部份熱量來(lái)破壞低密度水的多面體結(jié)構(gòu)。
?水的比熱容隨氣溫下降先降低后減小水的密度是什么它表示什么,在35°C時(shí)有個(gè)極小值,而絕大多數(shù)液體的比熱容隨氣溫下降而仍然減小。
在0至35°C之間,濕度下降造成水底的多面體結(jié)構(gòu)不斷被破壞,以便水份子做無(wú)序的運(yùn)動(dòng);隨著氣溫下降,多面體結(jié)構(gòu)越來(lái)越少,水變得放熱能力在減少。氣溫達(dá)到35°C時(shí),水底多面體結(jié)構(gòu)破壞殆盡,水的比熱容開始表現(xiàn)得類似通常液體了。
水的比熱容與濕度。圖源:
?水的壓縮率——加壓以后,降低的容積與衣原體積之比——隨氣溫下降先降低后減小,在46°C時(shí)有個(gè)極小值,而絕大多數(shù)液體的壓縮率隨氣溫下降而仍然減小。
隨著氣溫下降,46°C之前,水表現(xiàn)得難于被壓縮,這是由于低密度水的結(jié)構(gòu)漸趨解體,萊西度水比列越來(lái)越高。氣溫達(dá)到46°C以后,水底幾乎只有無(wú)序的青州度水,行為類似普通液體,氣溫越高越易被壓縮。
比熱容彰顯的是微觀結(jié)構(gòu)數(shù)量的變化,壓縮率彰顯的是分子堆積的松緊程度,兩者極小值不落在同一氣溫,是正常的。
?水比絕大多數(shù)液體無(wú)法被壓縮。
這是電負(fù)性帶給水分子之間強(qiáng)烈的吸引力引起的,尤其是對(duì)于萊州度水。
?高壓下水分子更適于擴(kuò)散。
高壓可破壞多面體有序結(jié)構(gòu),水份子排列越無(wú)序,越適于擴(kuò)散。
?水受熱膨脹,加壓,更膨脹……
加壓使水更無(wú)序,從而便于膨脹。
不再列出水的更多反常性質(zhì)給以解釋了。反正,水份子有兩種排列形式,這個(gè)理論與實(shí)驗(yàn)相符,且能一致地解釋水的反常性質(zhì)。
水的奇特性質(zhì)的奧秘開始浮出水面,只不過(guò),這讓水變得更古怪。
主要參考資料
New,2018,238,3180,26-29New,2010,205,2746,32-.Rev.2016,116,7463?ofwaterToday,2017,70,18-21數(shù)學(xué),2010,39,79-84本文受科普中國(guó)·星空計(jì)劃項(xiàng)目扶植出品:中國(guó)文聯(lián)科普部監(jiān)制:中國(guó)科學(xué)技術(shù)出版社有限公司、北京中科星河文化傳媒有限公司
#知識(shí)創(chuàng)作人#
